
已知反应A2(g)+2B2(g)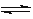 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石。已知12g石墨完全转化为金刚石时,要吸收E kJ的能量,下列说法正确的是( )
A.金刚石与石墨互为同位素 B.石墨不如金刚石稳定
C.金刚石不如石墨稳定 D.等质量的石墨与金刚石完全燃烧,石墨放出的能量多
查看答案和解析>>
科目:高中化学 来源: 题型:
为减少汽车尾气对大气造成的污染,目前市场上推出了使用乙醇汽油(在汽油中加入适量乙醇)的汽车。下列叙述错误的是
A.乙醇汽油是一种化合物 B.汽车使用乙醇汽油可以减少有害气体的排放
C.乙醇充分燃烧生成CO2和H2O D.用粮食发酵可制得乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是
A.碳酸钙与稀硝酸反应: CaCO3+2H+ = Ca2++ CO2↑+H2O
B.金属钠与水反应: 2Na +2H2O =2Na+ +2OH-+ H2↑
C.铁溶于稀硫酸中: 2Fe+6H+ = 2Fe3++3H2↑
D.氢氧化钡溶液中滴加稀硫酸:Ba2+ + SO42-=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使上述反应发生N2+3H2 2NH3。下列说法正确的是( )
2NH3。下列说法正确的是( )
A.达到化学平衡时,N2完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应速率都为零
查看答案和解析>>
科目:高中化学 来源: 题型:
综合利用CO2对 环境保护及能源开
环境保护及能源开 发意义重大。
发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是 。
a. 可在酸性氧化物中寻找 
b . 可在碱性氧化物中寻找
c . 可在ⅠA、ⅡA族元素形成的
. 可在ⅠA、ⅡA族元素形成的 氧化物中寻找
氧化物中寻找
d. 可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是: 在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是 。
在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是 。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:

已知:

① 反应Ⅱ是_____反应(填“吸热”或“放热”)。
② 反应A的热化学方程式是 。
 (4)如图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3
(4)如图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3 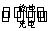 Na2S4+3NaBr 闭合开关K时,b极附近先变红色。则
Na2S4+3NaBr 闭合开关K时,b极附近先变红色。则
①负极反应式为:
②当有0.02 mol Na+通过离子交换膜时,b电极上析出的气体体积为 mL
③闭合K后,b电极附近的pH (填变大、变小或不变);
同时a电极反应式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com