
【题目】下列分散质微粒直径在1nm至100nm之间的是( )
A.氯化钠溶液B.氢氧化铁胶体C.氢氧化钙悬浊液D.水
科目:高中化学 来源: 题型:
【题目】已知还原性I﹣>Fe2+>Br﹣ , 下列离子方程式正确的是( )
A.将少量Cl2通入FeBr2溶液中:Cl2+2Br﹣═Br2+2Cl﹣
B.将足量Cl2通入FeBr2溶液中:2Fe2++2Br﹣+2Cl2═2Fe3++Br2+4Cl﹣
C.将少量Cl2通入FeI2溶液中:2Fe2++2I﹣+3Cl2═2Fe3++2I2+6Cl﹣
D.将672mLCl2(标况)通入250mL 0.1molL﹣1的FeI2溶液中:2Fe2++10I﹣+6Cl2═12Cl﹣+5I2+2Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置进行木炭粉和浓硫酸的反应及其全部产物的检验。
已知:紫红色的酸性高锰酸钾溶液能与二氧化硫发生氧化还原反应,向酸性高锰酸钾溶液通入足量的二氧化硫气体,溶液的紫红色会完全褪去。
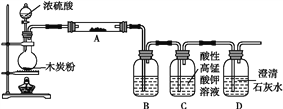
(1)组装好上述装置后,首先要进行的操作是________________。
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:_________________。
(3)装置A中试剂的化学式为______,装置B的作用是____________________________。
(4)实验时,可以说明生成二氧化碳的实验现象是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是
A. 过滤操作时,用玻璃棒搅拌漏斗内的液体,以加速过滤
B. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C. 萃取操作时,可以选用CCl4作为萃取剂从碘水中萃取碘
D. 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钻、钙等多种化学物质。
请回答下列问题:
(1) 区分晶体硼和无定形硼最可靠的科学方法为___________。第二周期元素的电负性按由小到大的顺序排列,B元素排在第__________位,其基态原子价层电子的电子云轮廊图为 _______________。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为____________,Si原子的杂化类型为__________________。
(3) N元素位于元素周期表_____________区;基态N原子中,核外电子占据最高能级的电子云有______伸展方向。

(4)[Co(NH3)6]3+的几何构型为正八面体形,Co在中心。
①[Co(NH3)6]3+中,1个Co提供_______________个空轨道。
②若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成_____________种不同的结构形式。
(5)—种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有___________________个。
②若Ca与O之间的最短距离为α pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g· cm-3(用含α、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是( )
A、2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
B、1mol 苯乙烯中含有的碳碳双键数为4NA
C、0.1mol CnH2n+2中含有的碳碳单键数为0.1n NA
D、标准状况下,2.24L CHCl3含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分离(括号内的物质为杂质)的方法错误的是( )
A.硝基苯(苯)--蒸馏
B.乙烯(SO2)--氢氧化钠溶液
C.己烷(己烯)--溴水,分液
D.乙酸乙酯(乙醇)--碳酸钠溶液,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化石燃料加工的说法正确的是
A.石油裂化主要得到乙烯
B.石油分馏是化学变化,可得到汽油、煤油等
C.煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
D.煤的气化是物理变化,是高效、清洁地利用煤的重要途径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com