
【题目】一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)![]() zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,当恒温下将密闭容器的容积扩大到两倍再达到平衡后,测得A浓度为0.3 mol·L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,当恒温下将密闭容器的容积扩大到两倍再达到平衡后,测得A浓度为0.3 mol·L-1,则下列叙述正确的是
A. 平衡向正反应方向移动 B. x+y<z
C. C 的体积分数降低 D. B的转化率提高
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离的 c(H+)=1×10-13mol·L-1,该溶液可能是 ( )
①SO2 水溶液 ② NH4Cl 溶液 ③ NaNO3 溶液 ④ NaOH 溶液
A. ①④ B. ①② C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①乙酸乙酯和碳酸钠溶液②甲醇和乙醇③溴化钠和溴水三组混合物,分离它们的正确方法依次是( )
A. 分液 蒸馏 萃取 B. 蒸馏 萃取 分液
C. 分液 萃取 蒸馏 D. 萃取 蒸馏 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是________(填标号)。
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L-1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为_______,制得等量H2所需能量较少的是________。
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)![]() COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率α1=________%,反应平衡常数K=________。
②在620 K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率α2_______α1,该反应的ΔH________0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是________(填标号)。
A.H2S B.CO2 C.COS D.N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
![]()
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水中溶解度 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙 酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷却至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分液出来的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)装置B的名称是:_____________________。
(2)在洗涤操作中,第一次水洗的主要目的是:_________________________;
第二次水洗的主要目的是:__________________________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:___________________________。
(5)实验中加入少量无水硫酸镁的目的是:_________________________________。
(6)在蒸馏操作中,仪器选择及安装都正确的是:_____________(填标号)。
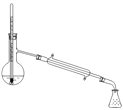

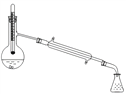
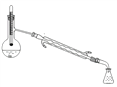
a b c d
(7)本实验的产率是:_________。
A.30 % B.40% C.50% D.60%
(8)在进行蒸馏操作时,若从130 ℃开始收集馏分,产率偏_________(填“高”或者“低”)。原因是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年中国汽车销量大幅增长,同时也带来了严重的空气污染.汽车尾气装置中,气体在催化剂表面吸附与解吸的过程如图所示,下列说法正确的是( ) 
A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.NO和O2必须在催化剂表面才能反应
D.催化转化总反应为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中,反应A+2B![]() C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是

A. 反应的平衡常数:①<② B. 反应A+2B![]() C的△H >0
C的△H >0
C. 实验②平衡时B的转化率为60% D. 实验③平衡时c(C) = 0.04 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )
2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )
A. 在有催化剂存在的条件下,反应放出的热量为92.4 kJ
B. 有无催化剂该反应放出的热量都为92.4 kJ
C. 若再充入1 mol H2,到达平衡时放出的热量应为92.4 kJ
D. 反应放出的热量始终小于92.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与环境、工农业生产等密切相关,下列叙述正确的是( )
A.光化学烟雾与大量排放碳氢化合物和氮氧化合物有关
B.将草木灰和硫酸铵混合施用,肥效更高
C.棉花的主要成分是纤维素,石英玻璃、陶瓷和水泥均属于硅酸盐产品
D.硫酸工业尾气未经处理就直接排放,将直接导致“温室效应”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com