
 $→_{盐酸}^{Fe}$
$→_{盐酸}^{Fe}$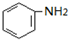 (苯胺易被氧化)
(苯胺易被氧化)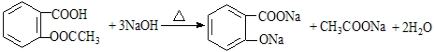 .
.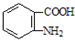 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)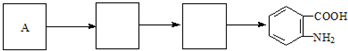
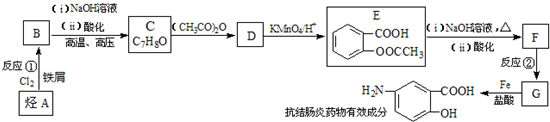
分析 C发生信息(a)中的反应生成D,D发生氧化反应生成E,结合C的分子式与E的结构简式,可知C的结构简式为 ,则D为
,则D为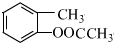 ,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为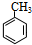 ,B为
,B为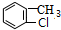 ;E与氢氧化钠反应、酸化得到F为
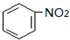
;E与氢氧化钠反应、酸化得到F为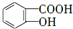 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为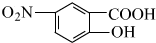 ,G发生还原反应得到抗结肠炎药物有效成分;
,G发生还原反应得到抗结肠炎药物有效成分;
(4)甲苯和浓硝酸发生取代反应生成邻甲基硝基苯,邻甲基硝基苯和酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸和Fe、HCl反应生成邻氨基苯甲酸,据此分析解答.
解答 解:C发生信息(a)中的反应生成D,D发生氧化反应生成E,结合C的分子式与E的结构简式,可知C的结构简式为 ,则D为
,则D为 ,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E;烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为 ,B为
,B为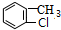 ;E与氢氧化钠反应、酸化得到F为
;E与氢氧化钠反应、酸化得到F为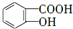 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为 ,G发生还原反应得到抗结肠炎药物有效成分,根据分析可知:A为
,G发生还原反应得到抗结肠炎药物有效成分,根据分析可知:A为 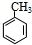 ,B为
,B为  .C为
.C为  ,D为
,D为 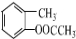 ,F为
,F为  ,G为
,G为 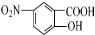 ,
,
(1)根据其结构简式确定分子式为:C7H7O3N;烃A为 ,其名称为甲苯;反应②为F(
,其名称为甲苯;反应②为F(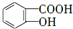 )在浓硫酸、浓硝酸加热条件下发生反应生成G
)在浓硫酸、浓硝酸加热条件下发生反应生成G ,该反应为取代反应,
,该反应为取代反应,
故答案为:C7H7O3N;甲苯;取代反应;
(2)①A.羧基、氨基与水分子之间可以形成氢键,其水溶性比苯酚好,故A正确;
B.含有氨基和羧基,所以能发生聚合反应,不能发生消去反应,故B错误;
C.该有机物分子中只含有1个苯环能够与氢气发生加成反应,则1mol该物质最多可与3mol H2发生反应,故C错误;
D.酚羟基和羧基具有酸性、氨基具有碱性,所以该物质既有酸性又有碱性,故D正确;
故答案为:AD;
②E中酯基和羧基都与NaOH反应,该反应的化学方程式为: ,
,
故答案为: ;
;
(3)其同分异构体符合下列条件:
A.遇FeCl3溶液有显色反应,说明含有酚羟基;
B.分子中甲基与苯环直接相连;
C.苯环上共有三个取代基,三个取代基分别是硝基、甲基和酚羟基,
若硝基和甲基处于邻位( ●为甲基可能的位置),有4种结构;
●为甲基可能的位置),有4种结构;
若硝基和甲基处于间位(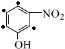 ●为甲基可能的位置),有4种结构;
●为甲基可能的位置),有4种结构;
若硝基和甲基处于对位(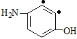 ●为甲基可能的位置),有2种结构,所以符合条件的有4+4+2=10种同分异构体,
●为甲基可能的位置),有2种结构,所以符合条件的有4+4+2=10种同分异构体,
故答案为:10;
(4)甲苯和浓硝酸发生取代反应生成邻甲基硝基苯,邻甲基硝基苯和酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸和Fe、HCl反应生成邻氨基苯甲酸,其合成路线为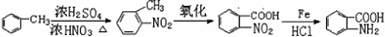 ,则两种中间产物的结构简式为:
,则两种中间产物的结构简式为: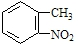 、
、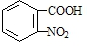 ,
,
故答案为: ;
; .
.
点评 本题考查有机物的合成,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查学生分析判断及知识综合运用能力,难点是合成路线设计和同分异构体种类判断,注意题给信息的正确筛取和运用,题目难度中等.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸甲酯 | B. | 甲酸乙酯 | C. | 乙酸乙酯 | D. | 乙酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
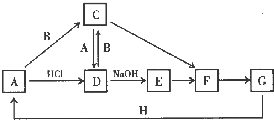 A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去).A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素.
A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去).A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com