
【题目】A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为__________________,E原子核外有_____个未成对电子,五种元素中电负性最大的是___________(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是______(填标号)。
A.中心原子的价层电子对数目相等B.都是非极性分子C.中心原子的孤电子对数目相等D.都含有极性键E.都能与Na2O反应F.固态时晶体类型不同
(4)D在空气中燃烧的产物分子构型为______。固体DB3中存在如图(b)所示的三聚分子,该分子中D原子的杂化轨道类型为________。

【答案】第三周期ⅥA族 2 O H2SO4 DE V形 sp3
【解析】
A、B、C、D、E为原子序数依次增大的五种前四周期元素。由A的核外电子总数与其周期数相同可知,A为H元素;由B的价电子排布式为nsnnpn+2可知,B的价电子数为6,则B为O元素;短周期元素C和D为同周期不相邻的元素,由C是同周期元素中离子半径最小的元素可知,C为Al元素;由D元素最外层有两个未成对电子可知,D为S元素;由E位于元素周期表的第四周期第IVB族可知,E为Ti元素。
(1)D为S元素,位于元素周期表第三周期ⅥA族;E为Ti元素,基态原子的价电子排布式为3d24s2,有2个未成对电子;元素的非金属性越强,电负性越大,五种元素中,O元素非金属最强,则O元素的电负性最大,故答案为:第三周期ⅥA族;2;O;
(2)由H、O、S三种元素形成的常见三元化合物中具有强氧化性的是硫元素的最高价氧化物对应水化物硫酸,化学式为H2SO4,故答案为:H2SO4;
(3)A.水分子中氧原子的价层电子对数为4,三氧化硫分子中硫原子的价层电子对数为3,中心原子的价层电子对数目不相等,故错误;
B.水分子的空间构型为V形,结构不对称,为极性分子,故错误;
C.水分子中氧原子的孤对电子对数为2,三氧化硫分子中硫原子的孤对电子对数为0,中心原子的孤对电子对数目不相等,故错误;
D.水分子中含有的H、O键为极性键,三氧化硫分子中含有的S、O键为极性键,故正确;
E.水与氧化钠反应生成氢氧化钠,三氧化硫与氧化钠反应生成硫酸钠,水和三氧化硫都能与氧化钠反应,故正确;
F.固态时,水和三氧化硫都是分子晶体,分子晶体类型相同,故错误;
DE正确,故答案为:DE;
(4)D为S元素,硫在空气中燃烧生成二氧化硫,二氧化硫分子中价层电子对数为3,孤对电子对数为1,则空间构型为V形;由图可知,三聚三氧化硫分子中每个硫原子连接4个氧原子,形成四面体结构,则硫原子的杂化方式为sp3杂化,故答案为:V形,sp3。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c)表示止水夹。
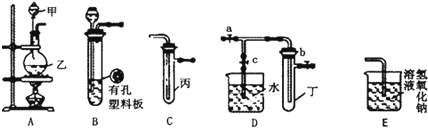
请按要求填空:(可供选择的试剂有:Cu片,MnO2粉末,浓硝酸,稀硝酸,浓硫酸,浓盐酸,氢氧化钠溶液,酚酞)
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水加入到滴有酚酞的NaOH溶液中,观察到溶液褪色,甲同学给出的结论是氯水溶于水生成了酸,将NaOH中和后溶液褪色。
a.写出制取氯气的化学方程式:___。
b.乙同学认为甲同学的结论不正确,他认为褪色的原因可能是___。
c.如何验证甲、乙两同学的结论(写出所加试剂,现象,结论):___。
(2)B、D、E装置相连后,可制得NO2并进行有关实验。
①B中发生反应的化学方程式为___。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹___,再打开止水夹___,使烧杯中的水进入试管丁的操作是___。
③试管丁中的NO2与水充分反应,若向试管内缓缓通入一定量的O2,直到试管全部充满水,则所得溶液中的溶质的物质的量浓度是___(气体按标准状况计算,结果保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3 的原理________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
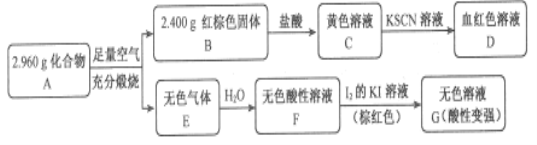
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),写出该反应的离子方程式_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各题的填空:
(1)葡萄糖分子式_____。葡萄糖的检验方法有:A、在碱性、加热的条件下,与银氨溶液反应析出银。该反应被称为葡萄糖的银镜反应。B、在碱性、加热的的条件下,与新制氢氧化铜反应产生现象为___。
(2)能使蛋白质发生变性有重金属盐、甲醛(福尔马林溶液)、强酸强碱、紫外线、加热等,误食重金属离子后应喝大量___解毒。
(3)青霉素是重要的抗生素即消炎药,在使用之前要进行_________________,以防 止过敏反应的发生。维生素C又称抗坏血酸,是一种水溶性维生素,具有酸性和还原性,广泛存在于 ___________。
(4)碘是人体必需的微量元素,有“智力元素”之称。缺碘会造成________,补碘过量会造成甲状腺功能亢进。在食物中,海带、海鱼等海产品中含碘最多。加碘盐中添加的是 _____(填化学式)。
(5)铁是人体中必需微量元素中含量最多的一种。缺铁会发生____含铁较多的食物有动物内脏、动物全血、肉类、鱼类、蛋类等。
(6)羊毛、蚕丝属于蛋白质。检验蛋白质的简单方法:_________。
(7)某蛋白质分子中含铁0.28%,测知该分子的相对分子质量为20000。则该分子中含铁原子___个。(已知铁的相对原子质量为56)。
(8)将标准状况下5.6L HCl气体通入50ml水中充分吸收,然后加水冲稀至500ml,此时盐酸的物质的量浓度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,只改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g)的影响如图所示,下列说法正确的是( )
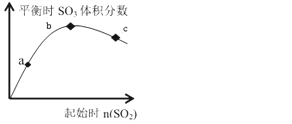
A. 反应a、b、c点均为平衡点,且b点时SO2的转化率最高
B. b点时SO2与O2 的物质的之比约为2:1
C. a、b、c 三点平衡常数: Kb>Kc>Ka
D. a、b、c 三点反应速率大小为: vb>vc>va
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,在充电和放电时,其电池反应为Mg+2MnF3![]() 2MnF2+MgF2。下列说法不正确的是( )
2MnF2+MgF2。下列说法不正确的是( )
A. 放电时,镁为负极材料
B. 放电时,电子从镁极流出,经电解质流向正极
C. 充电时,阳极的电极反应式为:MnF2+F--e-=MnF3
D. 充电时,外加直流电源负极应与原电池的Mg极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不能达到相应实验目的的是
实验方案 |
|
|
|
|
实验目的 | A.制备乙酸乙酯 | B.制取新制的 Cu(OH)2溶液 | C.除去溴苯中的苯 | D.除去乙烯中的二氧化硫 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是相对分子质量为28的烃。以A为原料合成有机化合物D的方法如下图所示。

(1)A 的结构简式是_____________,A → B 的反应类型是_____________。
(2)B→C 反应的试剂及条件是_________________。
(3)C→D 反应的化学方程式是________________。
(4)写出C 和乙二酸在一定条件下合成高分子化合物的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )

A.平衡常数K=![]()
B.该反应在T1时的平衡常数比T2时的小
C.CO合成甲醇的反应为吸热反应
D.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com