
下列对各组离子或物质是否能够大量共存解释正确的是(双选)( )
| A | 常温常压下NH3、O2、H2、CO2 | 不能 |
| 共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 | |
| B | c(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO | 不能 |
| 共存 | 发生反应:3Fe2++NO | |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能 |
| 共存 | 发生反应:Cu2++2NH3·H2O===Cu(OH)2↓+2NH | |
| D | 溶液中:Al3+、Na+、SO | 可以 |
| 共存 | 不能发生反应 |
科目:高中化学 来源: 题型:
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒.降脂等药效,主要酸性物质为苹果酸.苹果酸在分离提纯后的化学分析如下:①相对分子质量不超过150,完全燃烧后只生成CO2和H2O,分子中C、H质量分数分别为w(C)=35.82%.w(H)=4.48%;②1mol该酸与足量的NaHCO3反应放出44.8L CO2,与足量的Na反应放出33.6L H2(气体体积均已折算为标准状况);(已知:RCOOH+NaHCO3→RCOONa+CO2+H2O,2RCOOH+2Na→2RCOONa+H2,2ROH+2Na→2RONa+H2③该分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境.回答下列问题:
(1)苹果酸的分子式为 ,分子中有 个羧基.
(2)写出苹果酸的结构简式 .
(3)若一个碳上边有四个不同的基团,就可以认为是手性碳原子,在苹果酸的结构简式中是否存在手性碳原子,若有请用*符号标出.标在(2)小题上.
查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:____________________________________。
(2)[2014·全国新课标Ⅱ,27(2)(3)]①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为____________________。
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的一组离子是( )
A.H+、I-、NO 、SiO
、SiO B.NH
B.NH 、OH-、Cl-、HCO
、OH-、Cl-、HCO
C.K+、SO 、Cu2+、NO
、Cu2+、NO D.Al3+、Mg2+、SO
D.Al3+、Mg2+、SO 、CO
、CO
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是(双选)( )
A.1.0 mol·L-1的KNO3溶液:NH 、Fe2+、Cl-、SO
、Fe2+、Cl-、SO
B.1.0 mol·L-1的NaAlO2溶液:Cl-、HCO 、K+、Ba2+
、K+、Ba2+
C.1.0 mol·L-1的FeCl2溶液:NO 、Na+、K+、ClO-
、Na+、K+、ClO-
D.澄清透明的溶液:Cu2+、SO 、Mg2+、Cl-
、Mg2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值。下列说法正确的是( )
A.标准状况下,22.4 L Cl2中含有的氯原子数目为2NA
B.25℃时,在pH=2的1.0 L H2SO4溶液中含有的H+数目为0.02NA
C.1 L 0.1 mol·L-1 CuSO4溶液中含有的Cu2+数目为0.1NA
D.44 g CO2中含有的C===O键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值。下列说法正确的是
( )
A.1 L 0.1 mol·L-1 AlCl3溶液中Al3+的数目为0.1NA
B.常温常压下,17 g NH3中含有的原子总数为4NA
C.1 mol羟基中含有10NA个电子
D.常温常压下,2.24 L CH4中含有的碳原子总数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验可实现鉴别目的的是( )
A.用KOH溶液鉴别SO3(g)和SO2
B.用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和CH3COONa溶液
D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) 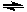 nY(g)ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示,下列说法正确的是( )
nY(g)ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示,下列说法正确的是( )
A.m>n B.体积不变,温度升高,平衡向逆反应方向移动
C.Q<0 D.温度不变,压强增大,Y的质量分数减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com