
| A. | ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 多电子原子中,在离核较近的区域内运动的电子能量较低 | |
| D. | 两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键 |
分析 A、ⅡA族元素的原子变成离子,失去1个电子层;
B、ⅢB族到ⅡB族为过渡金属元素;
C、在离核较近的区域内运动的电子能量较低;
D、两个非金属元素原子间只可能形成共价键,但是含金属元素的化合物中不一定含离子键,如氯化铝为共价化合物,不含离子键.
解答 解:A、金属原子失去电子形成阳离子,电子层减少,则ⅡA族元素的阳离子与上一周期稀有气体元素的原子具有相同的核外电子排布,故A正确;
B、从ⅢB族到ⅡB族10个纵行为副族及第Ⅲ族元素,均为金属元素,故B正确;
C、多电子原子中,在离核较远的区域内运动的电子能量较高,在离核较近的区域内运动的电子能量较低,故C正确;
D、含金属元素的化合物如氯化铝中含共价键,故D错误;
故选D.
点评 本题多角度考查元素周期表与周期律知识,题目难度中等,侧重于基础知识的综合理解与运用的考查,注意相关基础知识的积累.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
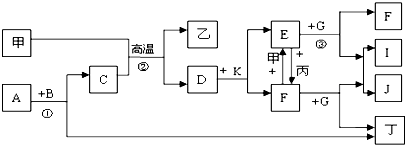
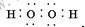 、甲在周期表中位置是第四周期第Ⅷ族;
、甲在周期表中位置是第四周期第Ⅷ族;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
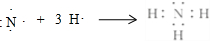 .
.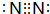 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ①⑤⑥ | C. | ②③④ | D. | ①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
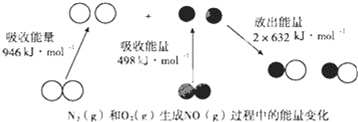
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
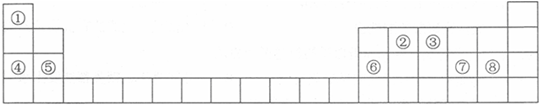
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com