

 ��
�� +HBr��
+HBr�� ����һ��ҽҩ�м��壮����ƺ�������������ȩ��
����һ��ҽҩ�м��壮����ƺ�������������ȩ�� ���ϳ�D������ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ��������
���ϳ�D������ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ�������� ���� ��1�������к���-COCl����������ˮ��������Ȼ����Ȼ��ⶼ�����������Ʒ�Ӧ��
��2��������I����Ľṹ��֪����Ӧ�ٷ���ȡ����Ӧ��ͬʱ������HBr��
��3����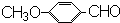 �ϳ�
�ϳ�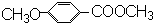 ���Ƚ�ȩ������Ϊ�Ȼ���Ȼ�����Ȼ��ʹ�֮�䷢��������Ӧ���ɣ�
���Ƚ�ȩ������Ϊ�Ȼ���Ȼ�����Ȼ��ʹ�֮�䷢��������Ӧ���ɣ�
��� �⣺��1�������к���-COCl����������ˮ��������Ȼ����Ȼ��ⶼ�����������Ʒ�Ӧ������1mol���������뺬2mol NaOH��ˮ��Һ��Ӧ��
�ʴ�Ϊ��2��
��2��������I����Ľṹ��֪����Ӧ�ٷ���ȡ����Ӧ��ͬʱ������HBr����ѧ����ʽΪ��CH2=CH-CH2Br+ ��
�� +HBr��
+HBr��
�ʴ�Ϊ��CH2=CH-CH2Br+ ��
�� +HBr��
+HBr��
��3�� �ϳ�
�ϳ� �Ĺ���Ϊ���Ƚ�ȩ������Ϊ�Ȼ���Ȼ�����Ȼ��ʹ�֮�䷢��������Ӧ���ɣ��ϳ�·��Ϊ��
�Ĺ���Ϊ���Ƚ�ȩ������Ϊ�Ȼ���Ȼ�����Ȼ��ʹ�֮�䷢��������Ӧ���ɣ��ϳ�·��Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ϳɡ��л���ṹ�����ʣ��Ѷ��еȣ�������ѧ�����������Ŀ��飬�ؼ��������л�������ŵ����ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20% | B�� | 30% | C�� | 45% | D�� | 55% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ | |
| B�� | ��֪NaOH��aq��+HCl��aq��=NaCl��aq��+H2O��l����H=-57.3kJ/mol����40.0gNaOH��ϡ��Һ�������ȫ�кͣ��ų�57.3kJ������ | |
| C�� | CO��g����ȼ������283.0kJ/mol�����ʾCO��g����ȼ���ȵ��ȷ���ʽΪ2CO��g��+O2��g��=2CO2��g����H=-283.0kJ/mol | |
| D�� | ��֪2C��s��+2O2��g��=2CO2��g����H=akJ/mol��2C��s��+O2��g��=2CO��g����H=bkJ/mol����b��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
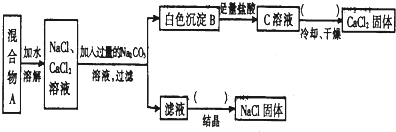
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.6 mol•L-1•min-1 | B�� | 0.9 mol•L-1•min-1 | ||
| C�� | 1.2 mol•L-1•min-1 | D�� | 1.8 mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȷ�Ӧ����ѧ����ʽΪ2Fe+Al2O3�T2Al+Fe2O3 | |
| B�� | ԭ����ǵ���ת��Ϊ��ѧ�ܵ�װ�� | |
| C�� | ��ɫֲ��Ĺ��������ʵ���˹�����ѧ�ܵ�ת�� | |
| D�� | �ȼҵ�õ�ⱥ��ʳ��ˮ���Ʊ������ͻ����ǽ���ѧ��ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪A��B��C��D��X��Y��ԭ���������������ǰ20��Ԫ�أ�����A��D��ԭ������ �����ŵģ�A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�X��Yλ��ͬһ���壬
��֪A��B��C��D��X��Y��ԭ���������������ǰ20��Ԫ�أ�����A��D��ԭ������ �����ŵģ�A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�X��Yλ��ͬһ���壬�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba2+��K+��OH-��SO42- | B�� | Fe3+��NO3-��Na+��OH- | ||
| C�� | H+��Na+��Cl-��SO42- | D�� | K+��SO42-��HCO3-��H+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com