
【题目】X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化:
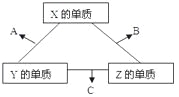
一个B分子中含有的Z原子个数比C分子少1个,B、C 两种分子中的电子数均等于10。
请回答下列问题:
(1)X元素在周期表中的位置是________________.
(2)B分子的电子式为________________。分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在_______________。
(3)已知Y+Z→C是一个可逆反应,其平衡常数表达式为_______________。有甲、乙两容器,容器容积固定,乙容器容积可变。一定温度下,在甲中加入2,molY、3molZ,反应达到平衡时生成C的物质的量为mmol。相同温度下,在乙中加入4 mol Y、6 mol Z,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成C的物质的量为________mol(从下列各项中选择,只填字母,下同);若乙的容积与甲的容积始终相等,乙中反应达到平衡时,生成C的物质的量为________mol。
A.小于m
B.等于m
C.在m~2m之间
D.等于2m
E.大于2m
(4)Y的最高价氧化物的水化物为W,其溶液呈黄色,其原因是________________(写化学方程式);W与C在适当条件下被W吸收生成一种盐Q,该盐的水溶液pH<7,其原因是(写出离子方程式)______________。
【答案】(1)2周期,ⅥA族;
(2)![]() 氢键(3)D E
氢键(3)D E
(4)NH3+HNO3=NH4NO3;NH4++H2O![]() NH3
NH3![]() H2O+H+(各2分)
H2O+H+(各2分)
【解析】试题分析:短周期中形成无色气体单质的只有H2、N2、O2(稀有气体除外),B、C两种分子中的电子数均等于10,则B、C为H2O、NH3的一种,且一个B分子中含有的Z原子个数比C分子中少1个,B为H2O,C为NH3,由转化关系可知,Z为氢,故A为NO,X为氧,Y为氮,
(1)O元素的质子数为8,位于第二周期VIA族;
(2)水分子的电子式为![]() ;氧元素、氟元素电负性很强,水分子之间、氨气分子之间存在氢键,故它们的沸点高于同主族其它元素氢化物;
;氧元素、氟元素电负性很强,水分子之间、氨气分子之间存在氢键,故它们的沸点高于同主族其它元素氢化物;
(3)可逆反应N2+3H2![]() 2NH3,其平衡常数表达式为K=c2(NH3)/[c(N2)×c3(NH3)]。若甲的体积为VL,另有一个体积为2VL的固定体积的容器丙,4 mol N2、6 mol H2,在此容器中达到平衡时NH3的物质的量为2mmol,气体的压强也与甲相同,故乙容器内平衡时生成NH3的物质的量为2mmol,答案为D;如果乙的体积与甲的体积相同,则应将丙的体积缩小为VL,此时平衡正向移动,平衡时生成NH3的物质的量大于2m,答案为E;
2NH3,其平衡常数表达式为K=c2(NH3)/[c(N2)×c3(NH3)]。若甲的体积为VL,另有一个体积为2VL的固定体积的容器丙,4 mol N2、6 mol H2,在此容器中达到平衡时NH3的物质的量为2mmol,气体的压强也与甲相同,故乙容器内平衡时生成NH3的物质的量为2mmol,答案为D;如果乙的体积与甲的体积相同,则应将丙的体积缩小为VL,此时平衡正向移动,平衡时生成NH3的物质的量大于2m,答案为E;
(4)O、N、H三种元素可组成一种强酸为HNO3,NH3在适当条件下被HNO3吸收生成一种盐为NH4NO3,该盐的水溶液中NH4+离子水解:NH4++H2ONH3H2O+H+,破坏水的电离平衡,溶液呈酸性,故pH<7。


科目:高中化学 来源: 题型:
【题目】
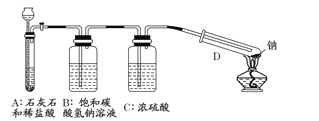
(1)该装置中饱和碳酸氢钠溶液的作用是 ,浓硫酸的作用是 。
(2)从试剂瓶中取出的金属钠,必须经过必要的操作,方可进行后续的实验,该必要的操作是 。
(3)放进试管中的金属钠在加热之前,必须进行的操作是 。
(4)用酒精灯在试管底部加热,钠在充满二氧化碳气体的试管里剧烈地燃烧,产生大量的白烟。试管底部有黑色物质生成。试管冷却后,试管壁上附着一层白色物质。往试管中加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现,则试管壁上附着的白色物质是 。然后将滤纸上的黑色物质移入小试管中,加少量浓硫酸,加热,产生有刺激性气味的二氧化硫气体和另一种无色常见气体。则该黑色物质与浓硫酸共热的化学反应方程式为 。
(5)据(4)中现象,试写出钠与二氧化碳反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述合理的是( )
A. 用干燥的pH试纸检测碳酸钠溶液、氯水、稀醋酸的pH值
B. 铜与浓硫酸反应时,可用蘸有浓溴水的棉花放在导管口吸收逸出的气体
C. 需用某浓度的NaOH溶液450 mL,则配制时应选用450 mL的容量瓶
D. 将液溴、浓硝酸保存在棕色试剂瓶中,放置于冷暗处
查看答案和解析>>
科目:高中化学 来源: 题型:
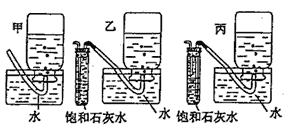
【题目】在呼吸面具和潜水艇中可用过氧化钠作供氧剂,某课外活动小组设计了如下实脸装置,以证明过氧化钠可作供氧剂。装置A、B、C中盛装的试剂,可供选择的为:饱和NaHCO3溶液、CaCO3固体,NaOH 溶液,39gNa2O2固体。据下述装置回答问题:

(1)盛盐酸的仪器名称_________________。
(2)B瓶中装__________,作用是_________________,反应的离子方程式_________________。
(3)若D中的石灰水出现出现轻微白色浑浊,请说明原因:_______________________。
(4)反应完毕时,若测得E中收集到的气体为520 mL,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值_________(填“大”或“小”),相差约_______mL,这是由于___________。
(5)为了使装置D部分更安全、合理,可将装置D改为下列________装置(用甲、乙、丙回答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁—次氯酸盐燃料电池的工作原理如右图所示,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-

下列有关说法正确的是( )
A.电池工作时,c溶液中的溶质一定是MgCl2
B.负极反应式:ClO--2e-+H2O=Cl-+2OH-
C.电池工作时,OH-向b电极移动
D.b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素单质从F2到I2,在常温、常压下的聚集状态由气态、液态到固态的原因是 ( )
A. 原子间的化学键键能逐渐减小
B. 范德华力逐渐增大
C. 原子半径逐渐增大
D. 氧化性逐渐减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com