
反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是
2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是
A.v(A)=0.15 mol·L-1·min-1
B.v(B)=0.015 mol·L-1·s-1
C.v(C)=0.40 mol·L-1·min-1
D.v(D)=0.45 mol·L-1·min-1
科目:高中化学 来源:2014-2015学年湖北省高二上学期10月月考化学试卷(解析版) 题型:选择题
下列关于有机化合物的说法正确的是
A.分子式为C3H6O2的链状有机物中含有一个双键
B.1 mol甲烷与Cl2完全发生取代反应需2 mol Cl2
C.1 mol乙烯与Cl2完全发生加成反应需2 mol Cl2
D.乙醇与乙酸均能被酸性KmnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省绍兴市高一上学期期中化学试卷(解析版) 题型:选择题
将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数 变为2a%,此时该H2SO4的物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是
A.c2=2c1 B.c2>2c1 C.c2<2c1 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省绍兴市高一上学期期中化学试卷(解析版) 题型:选择题
下列说法错误的是
A.卢瑟福提出了带核的原子结构模型
B.已知PM2.5是指大气中直径≤2.5×10-6m的颗粒物,受PM2.5污染的大气不一定能产生丁达尔现象
C.借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有的非金属元素
D.并不是所有金属元素都可以用焰色反应来确定其存在
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市十校联合体高二上学期期中联考化学试卷(解析版) 题型:填空题
(16分)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸, 总反应为:
总反应为:
2CH3CHO + H2O === CH3CH2OH + CH3COOH。实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。
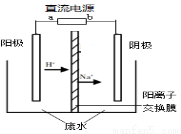
(1)若以甲醇燃料电池为该电解的直流电源,燃料电池中的电解液是氢氧化钠溶液,则燃料电池中b极的电极反应式为 。电池工作一段时间后,氢氧化钠溶液物质的量浓度 (填变大,变小或不变)
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。阳极电极反应如下:① 4OH- - 4e-== O2↑+ 2H2O;②
(3)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
(4)若直流电源使用新型的熔融碳酸盐燃料电池(MCFS),该电池以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650 ℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1∶1)直接作燃料,其工作原理如图所示。
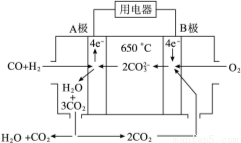
①B极发生______(填“氧化”或“还原”)反应,电极反应式 。
②以此电池电解足量的CuSO4溶液,当电池消耗1.12L(标准状况下)氧气时,则阴极产物的质量为_ _____ g。加入一定量的 可以让CuSO4溶液回复原状。
A、CuO B、Cu(OH)2 C、CuCO3 D、Cu
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市十校联合体高二上学期期中联考化学试卷(解析版) 题型:选择题
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子(硫单质参加化学反应时断键的过程)吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
A.-1780kJ/mol B. -1220 kJ/mol C.-450 kJ/mol D.+430 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市十校联合体高二上学期期中联考化学试卷(解析版) 题型:选择题
工业上利用可逆反应N2(g)+3H2(g)?2NH3(g)合成氨,下列叙述正确的是
A.恒温恒压条件下混合气体相对密度不再改变可以说明该反应已经达平衡状态
B.恒容通入氩气,使反应体系的压强增大,反应速率必定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.随着反应的进行,逆反应速率逐渐增大,正反应速率逐渐减小最后为0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市十校联合体高一上学期期中联考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.稀硫酸滴在铜片上:Cu + 2H+ == Cu2+ + H2 ↑
B.氢氧化镁溶于盐酸:OH-+H+ == H2O
C.铁跟稀硫酸反应:2Fe+6H+ ==2Fe3++3H2↑
D.铜和硝酸银溶液反应: Cu + 2Ag+ == 2Ag + Cu2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州市高二10月月考化学试卷(解析版) 题型:选择题
下列关于能量的变化及反应热的说法中正确的是 ( )。
A.任何化学反应都有反应热
B.有些化学键断裂时吸收能量,有些化学键断裂时放出能量
C.新化学键的形成不一定放出能量
D.有热量变化的反应一定有化学键的断裂与形成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com