
| 编号 | A | B | C | D |
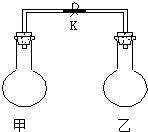
| 甲中气体 | H2S | H2 | NH3 | NO |
| 乙中气体 | SO2 | Cl2 | HCl | O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 相同温度下,一定体积的容器中气体压强与气体的物质的量成之比,气体的物质的量越大其压强越大,据此解答.
解答 解:设烧瓶的体积为V.
A.硫化氢与二氧化硫反生成硫单质和水,2H2S+SO2=3S↓+2H2O,反应后气体体积减小,剩余SO2气体体积$\frac{1}{2}$V;
B.氢气和氧气在常温下不反应,气压不变,剩余气体为2V;
C.氨气和氯化氢反应生成氯化铵,反应后气体压强为零,剩余气体为0;
D.一氧化氮和氧气化合会生成二氧化氮,即2NO+O2═2NO2,然后发生2NO2?N2O4,反应后气体体积减小,剩余O2气体体积为积$\frac{1}{2}$V,生成NO2体积V,剩余气体总体积约$\frac{3}{2}$V;
所以B中压强最大;
故选:B.
点评 本题考查了物质的性质及阿伏伽德罗定律,明确物质的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题

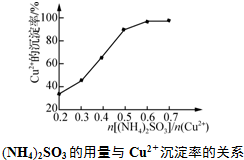 ,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.
,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )| A. | 电池工作时,K+向负极移动 | |
| B. | 电池工作时,Al电极周围溶液pH增大 | |
| C. | 正极反应为MnO4-+2H2O+3e-═MnO2+4OH- | |
| D. | 电池工作时,电子由Al经溶液流向Ni |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雷雨天气时产生少量NO | |
| B. | 往农田中施放铵态氮肥 | |
| C. | 豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨 | |
| D. | N2和H2在高温、高压和催化剂存在下合成氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2(CO):通过灼热的CuO粉末 | B. | Na2SO4溶液(Na2CO3):加盐酸 | ||
| C. | NaCl(NH4Cl):加热 | D. | NO2(NO):通入水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
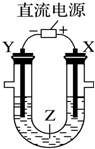
| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的铜离子浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 电解水制氢气时,Z可以是稀硫酸溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com