
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
分析 A.水晶的成分为二氧化硅;
B.SO2和CO2均与石灰水反应生成白色沉淀;
C.Fe(NO3)2 溶于稀盐酸,发生氧化还原反应生成铁离子;
D.硅酸盐用氧化物的形式表示,按照活泼金属的氧化物、较不活泼金属氧化物、二氧化硅、水排列,遵循原子守恒.
解答 解:A.水泥、玻璃都是硅酸盐制品,而水晶饰物的成分为二氧化硅,故A错误;
B.SO2和CO2均与石灰水反应生成白色沉淀,现象相同,不能鉴别,故B错误;
C.Fe(NO3)2 溶于稀盐酸,发生氧化还原反应生成铁离子,滴加KSCN 溶液,溶液为血红色,故C错误;
D.硅酸盐用氧化物的形式表示,按照活泼金属的氧化物、较不活泼金属氧化物、二氧化硅、水排列,遵循原子守恒,则Ca2Mg5Si8O22(OH)2写成氧化物的形式为2CaO•5MgO•8SiO2•H2O,故D正确;
故选D.
点评 本题考查物质的检验和鉴别,为高频考点,把握物质的性质、发生的氧化还原反应、硅酸盐及组成为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | 用pH试纸测溶液的pH时,需先用蒸馏水润湿试纸 | |
| C. | 0.2 mol/L的盐酸与等体积水混合后pH约为1 | |
| D. | 25℃时,pH=12的氨水溶液与pH=2的盐酸等体积混合后pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径依次增大 | B. | 单质的熔沸点逐渐升高 | ||
| C. | 卤离子的还原性逐渐减弱 | D. | 氢化物的热稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
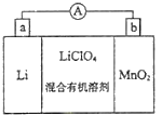 如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:
如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com