
 某化学小组进行Na2SO3的性质实验探究.
某化学小组进行Na2SO3的性质实验探究.| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
| n(SO${\;}_{3}^{2-}$ ):n(HSO${\;}_{3}^{-}$) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
分析 (1)①Na2SO3 溶液中亚硫酸钠具有还原性和溴单质反应生成硫酸钠;
②Na2SO3 溶液与硫化钠、硫酸溶液发生氧化还原反应生成淡黄色硫单质沉淀;
③Na2SO3 溶液水解显碱性,使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小红色褪去;
(2)①当吸收液中n(SO32-):n(HSO3-)=10:1 时,依据图表分析,溶液呈碱性;
A.依据溶液中电荷守恒分析;
B.溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大;
C.溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大;
②若n(SO32-):n(HSO3-)=3:2,反应物全部反应,根据写出的反应的离子方程式计算.
解答 解:(1)①滴入溴水后褪色,说明亚硫酸钠具有还原性,被溴单质氧化为硫酸钠,
故答案为:还原性;
②b中是滴入硫化钠溶液和稀硫酸,硫离子和亚硫酸根离子发生氧化还原反应生成淡黄色沉淀单质硫,发生反应的离子方程式是:SO32-+2S2-+6H+=3S↓+3 H2O;
故答案为:SO32-+2S2-+6H+=3S↓+3H2O;
③d中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去,在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),水解平衡左移,氢氧根离子浓度减小,红色褪去;
故答案为:在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去;
(2)①吸收液中n(SO32-):n(HSO3-)=10:1 时,依据图表数据分析判断,溶液呈碱性,亚硫酸钠物质的量大于亚硫酸氢钠
A.依据溶液中电荷守恒,c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-);故a正确;
B.溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大,离子浓度大小为:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故b错误;
C.溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大,离子浓度大小为:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故c正确;
故答案为:AC;
②若n(SO32-):n(HSO3-)=3:2,反应物全部反应,反应方程式为:5SO2+8NaOH=2NaHSO3+3Na2SO3+3H2O,则0.8mol NaOH溶液吸收了标准状况下的SO2物质的量为0.5mol,标准状况体积为0.5mol×22.4L/mol=11.2L;
故答案为:11.2.
点评 本题考查了物质性质实验验证方法的分析判断,溶液中离子浓度大小比较,溶液中电荷守恒应用,化学方程式的计算分析,盐类水解平衡的影响因素判断,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol NaCl 分子 | |
| B. | 质子数为 35、中子数为 45 的溴原子:${\;}_{35}^{45}$ Br | |
| C. | 硫离子的结构示意图: | |
| D. | NH4+ 的电子式: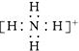 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白、红、白 | B. | 红、黑、白 | C. | 红、红、红 | D. | 白、黑、白 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 65g锌与足量稀硫酸反应产生的气体体积为22.4L | |
| B. | 标准状况下,以任意比混合的H2和CO气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA | |
| C. | 0.2mol H2O2在MnO2催化下充分反应生成O2的数目为0.2NA | |
| D. | 同温同压下,1mol H2在空气中充分燃烧,消耗O2的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
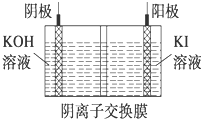 碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中.
碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中.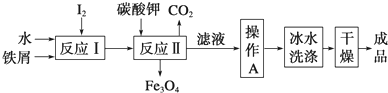
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
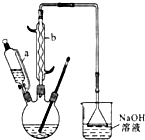 己二酸
己二酸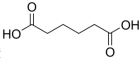 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下: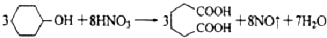
| 物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 | 相对分子质量 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度3.6g,可混溶于乙醇、苯 | 100 |
| 乙二酸 | 1.36g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时,1.44g,25℃时2.3g,易溶于乙醇,不溶于苯 | 146 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com