
����Ŀ����ͼ��ʾ����ˮ��![]() ��װ��
��װ��![]() ˮ���ݻ�Ϊ
ˮ���ݻ�Ϊ![]() ���Թ�
���Թ�![]() �г�����
�����![]() ��
��![]() �Ļ������(��״����)�����Թ�
�Ļ������(��״����)�����Թ�![]() ������ˮ��
������ˮ��![]() �С���ַ�Ӧ���Թ�
�С���ַ�Ӧ���Թ�![]() ��ʣ����������Ϊ
��ʣ����������Ϊ![]() ��
��
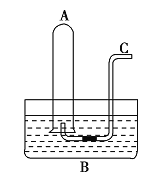
(1)��![]() ������ˮ��
������ˮ��![]() �з����ķ�ӦΪ________________________________________________���÷�Ӧ���������뻹ԭ����������Ϊ_____________��ԭ���������
�з����ķ�ӦΪ________________________________________________���÷�Ӧ���������뻹ԭ����������Ϊ_____________��ԭ���������![]() ��
��![]() �����ʵ���֮��Ϊ____________��
�����ʵ���֮��Ϊ____________��
(2)ͨ��������![]() ��ʣ��
��ʣ��![]() ������Թ�
������Թ�![]() �г���ͨ��������
�г���ͨ��������![]() �п��ܹ۲쵽��������_____________________________________________________________________________________________________��
�п��ܹ۲쵽��������_____________________________________________________________________________________________________��
(3)���Թ�![]() �г�������ʱֹͣͨ��������Ȼ���Թܴ�ˮ����ȡ����ˮ��
�г�������ʱֹͣͨ��������Ȼ���Թܴ�ˮ����ȡ����ˮ��![]() ����Һ�����ʵ���Ũ��Ϊ______
����Һ�����ʵ���Ũ��Ϊ______![]() (��ˮ����Һ��������Ϊ
(��ˮ����Һ��������Ϊ![]() )��
)��
���𰸡�![]()
![]()
![]() ��ɫ�����Ϊ����ɫ���Թ���Һ�治������ֱ��ȫ����������ͨ���������Թ���Һ�½�����������ɫ����
��ɫ�����Ϊ����ɫ���Թ���Һ�治������ֱ��ȫ����������ͨ���������Թ���Һ�½�����������ɫ���� ![]()
��������
(1) ![]() ���ˮ������Ӧ
���ˮ������Ӧ![]() �������ϼ۱仯�����ҳ�����������ԭ����չ�����㣻
�������ϼ۱仯�����ҳ�����������ԭ����չ�����㣻
(2)��Ӧ���Թ���ʣ��������NO��ͨ����������֮��Ӧ�����ɺ���ɫ![]() ����˷���
����˷���![]() ��ˮ�ķ�Ӧ�ٴ�����NO��ֱ�������굪��������ݴ�д��Ӧ����
��ˮ�ķ�Ӧ�ٴ�����NO��ֱ�������굪��������ݴ�д��Ӧ����
(3)����ˮ����Һ��������Ϊ![]() ������Һ�����ʵ���Ũ�ȣ��ؼ����ڸ��ݵ�ԭ���غ�
������Һ�����ʵ���Ũ�ȣ��ؼ����ڸ��ݵ�ԭ���غ�![]() ��
��
(1)�Թ�![]() ������ˮ��
������ˮ��![]() �У�NO����ˮ��Ӧ��
�У�NO����ˮ��Ӧ��![]() ��ˮ������Ӧ
��ˮ������Ӧ![]() ����Ϊ��
������![]() ��
��
![]() �У��������뻹ԭ����Ϊ
�У��������뻹ԭ����Ϊ![]() ��
��![]() ת�������ʱ����ԭ����ת���NOʱ����������������Ϊ1��2����Ϊ��1��2��
ת�������ʱ����ԭ����ת���NOʱ����������������Ϊ1��2����Ϊ��1��2��
���������![]() ����
����![]() ��
��![]() ������
������![]() ��
��
(2)�Թ�![]() ��ʣ���
��ʣ���![]() ����Ϊ
����Ϊ![]() ��ͨ������������Ӧ
��ͨ������������Ӧ![]() ������
������![]() ���ɺϲ���
���ɺϲ���![]() ����
����![]() ���ݴ�д��Ӧ����Ϊ����ɫ�����Ϊ����ɫ���Թ���Һ�治������ֱ��ȫ����������ͨ���������Թ���Һ�½�����������ɫ���壻
���ݴ�д��Ӧ����Ϊ����ɫ�����Ϊ����ɫ���Թ���Һ�治������ֱ��ȫ����������ͨ���������Թ���Һ�½�����������ɫ���壻
(3)�Թ��г�������ʱ�����ݵ�ԭ���غ�ɵ�![]() ����
����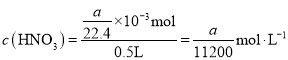 ������
������![]() ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪W��X��Y��ZΪ������Ԫ�أ�W��Zͬ���壬X��Y��Zͬ���ڣ�W����̬�⻯����ȶ��Դ���Z����̬�⻯����ȶ��ԣ�X��YΪ����Ԫ�أ�X�������ӵ�������С��Y�������ӵ������ԡ�����˵����ȷ���ǣ� ��
A.X��Y��Z��W��ԭ�Ӱ뾶���μ�С
B.W��XԪ�صĵ����ڳ����²���Ӧ
C.W����̬�⻯��ķе�һ������Z����̬�⻯��ķе�
D.��W��Y��ԭ���������5��������γɻ�����Ļ�ѧʽһ��ΪY2W3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;��ij�����Ի�ͭ��(��Ҫ�ɷ�Ϊ Cu2S�������� Fe2O3��SiO2 ������)Ϊԭ���Ʊ�������ˮ�ļ�ʽ̼��ͭ���������£�

��֪��
�ٳ����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�
�������� | Fe2�� | Fe3�� | Cu2�� | Mn2�� |
��ʼ���� | 7.5 | 2.7 | 5.6 | 8.3 |
��ȫ���� | 9.0 | 3.7 | 6.7 | 9.8 |
�� Ksp[Fe(OH)3]��4.0��10��38
(1)�ӿ�����ȡ�����ʣ����ʵ���������Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��__________����дһ�֣���
(2)����I�е���Ҫ�ɷ���MnO2��S��SiO2����д������ȡ����Ӧ������S�Ļ�ѧ����ʽ��______________��
(3)��������������ʱ������Լ�A����CuO�ȣ�����pH���ķ�ΧΪ_________������ A ����Һ�� pH��Ϊ4.0������Һ�� Fe3����Ũ��Ϊ_________mol/L��
(4)д����������(�� Mn2��)�����з�Ӧ�����ӷ���ʽ��_________________________��
(5)���ϰ���ʱ�������˵IJ���������________________��
(6)���ˢ�õ��ij�������ϴ�ӡ�������Եõ���ʽ̼��ͭ���жϳ����Ƿ�ϴ���IJ�����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��֪����3�ֳ���ԭ�ӣ�11H��21H��31H(��H��D��T)������2�ֳ�������ԭ�ӣ�35Cl��37Cl�������������γɵ��Ȼ�����ӵ���Է���������________�֡�
(2)������ͬ��H216O��D216O����������֮��Ϊ______��������֮��Ϊ________����������������ͬ��ͬѹ�����֮��Ϊ________������֮��Ϊ________��
(3)2 g AO32-����������������3.01��1022������A�����ԭ������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����AG��ʾ��Һ����ȣ������ʽΪAG=lg[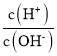 ]��298Kʱ����10mL0.1 molL-1 HX��Һ�еμ� 0.1molL-1NaOH ��Һ����Һ��AG��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵��������� �� ��
]��298Kʱ����10mL0.1 molL-1 HX��Һ�еμ� 0.1molL-1NaOH ��Һ����Һ��AG��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵��������� �� ��
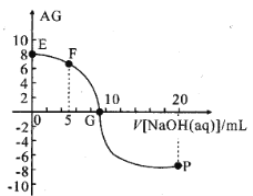
A.��ҺpH��AG�Ĺ�ϵʽΪAG=14-2pH
B.��G����Һ��c(Na+) = c(X-)
C.298KʱHX�ĵ��볣��Ka��1.0��10-5
D.��Һ��ˮ�����c(OH-) F��<P��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ����ѡ��3�����ʽṹ�����ʣ�
�ܼ��仯����������������Ҫ���ã��ش���������
(1)��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ________________��δ�ɶԵ�����Ϊ________________��
(2)�����[Co(NH3)4(H2O)2]Cl3������Ҫ������
��H2O�ķе�___ (��������������������)H2S��ԭ����_______��H2O��O���ӻ���ʽΪ_____��H2O��_____����(���������������Ǽ�����)��
��[Co(NH3)4(H2O)2]Cl3�е�Co3+��λ��Ϊ___�������ӵ����幹����___________��[Co(NH3)4(H2O)2]Cl3������������NH3���ӱ�Clȡ�������γɵ�[Co(NH3)2Cl2(H2O)2]3+�ļ����칹��������(�����ǹ�ѧ�칹)___________�֡�
(3)һ�����ܵľ�����ͼ������ÿ��Co2+����Χ������ӽ����Ҿ�����ȵ�Co2+����_____������������Co2+��O2-����С����Ϊacm����CoO�ľ����ܶ�Ϊ_______(�ú�NA��a�Ĵ���ʽ��ʾ�����g/cm3����֪:M(Co)=59g/mol��M(O)=16g/mol���谢���ӵ�����ΪNA)��
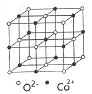
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ֱ�����ͼ��ʾװ�ö�ԭ��غ͵��ԭ������ʵ��̽������ش�
I.����ͼ��ʾװ�ý��е�һ��ʵ�顣
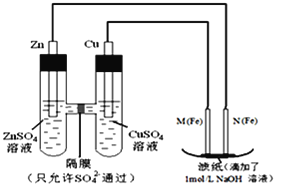
(1)N��������Ӧ�ĵ缫��ӦʽΪ_________.
(2)ʵ������У�SO42-______(������������������������������������)�ƶ���
II.����ͼ��ʾװ�ý��еڶ���ʵ�顣ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���塣�������Ϸ��֣��������(FeO42-)����Һ�г��Ϻ�ɫ��
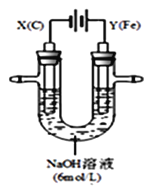
(3)�������У�X������Һ��pH______(����������������С������������)
(4)�������У�Y�������ĵ缫��ӦΪ_____________��4OH-- 4e-�� 2H2O + O2��
(5)����X���ռ���672mL���壬��Y���ռ���168mL����(��������Ϊ��״��ʱ�������)����Y�缫(���缫)��������______g
(6)�ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn�TFe2O3+ZnO+2K2ZnO2 �õ�����������ķ�Ӧ�ĵ缫��ӦʽΪ__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱͨ�����·�Ӧ�Ʊ������������������������ٷŵ������Ӷ��ε������ԭ������ͼ��ʾ(EMI+Ϊ�л�������)��

��Al2O3(s)+AlCl3(g)+3C(s) = 3AlCl(g)+3CO(g) ��H1= a kJ��mol-1
��3AlCl(g) = 2Al(l)+ AlCl3(g) ��H2= b kJ��mol-1
��Al2O3(s)+3C(s) = 2Al(l)+3CO(g) ��H3
����˵����ȷ����
A.�õ�صĵ���ʿ����Ȼ���ˮ��Һ���
B.Al2O3(s)+3C(s) = 2Al(l)+3CO(g) ��H3= (a-b) kJ��mol-1
C.�õ�س��ʱʯī�缫���Դ��������
D.�õ�طŵ�ʱ�ĸ�����Ӧ����ʽΪ ��Al-3e-+7AlCl4-=4Al2Cl7-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦX(g)��Y(g)![]() R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��830 ��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��v(X)��0.005 mol/(L��s)������˵����ȷ����
R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��830 ��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��v(X)��0.005 mol/(L��s)������˵����ȷ����
�¶�/�� | 700 | 800 | 830 | 1 000 | 1 200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 sʱ������c(Y)��0.76 mol/L
B. 830 ����ƽ��ʱ��X��ת����Ϊ80%
C. ��Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D. 1 200 ��ʱ��ӦR(g)��Q(g) ![]() X(g)��Y(g)��ƽ�ⳣ��K��0.4
X(g)��Y(g)��ƽ�ⳣ��K��0.4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com