
分析 (1)根据方程式,失电子的物质作负极;根据得失电子判断反应类型;电解质是反应物中可溶性的、得电子的物质;
(2)氢氧燃料电池工作时,负极发生氧化反应,正极发生还原反应,注意碱性电解质的条件下;
(3)铝热法炼铁的原理是用金属铝和铁的氧化物在高温下发生置换反应,属于热还原法的一种.
解答 解:(1)原电池中失电子的物质作负极,根据方程式知,铜作负极,比铜活泼性小的金属或导电的非金属作正极;铜失电子,发生氧化反应;电解质是反应物中可溶性的、得电子的物质,所以电解质是可溶性的银盐,可用硝酸银作电解质,
故答案为:铜;氧化;硝酸银;
(2)碱性氢氧燃料电池工作时,在负极上通入氢气,发生氧化反应,电极反应式为2H2-4e-+4OH-=4H2O,在正极上通入氧气,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
(3)铝热法炼铁的原理是用金属铝和铁的氧化物在高温下发生置换反应,以Fe2O3为例,反应的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
点评 本题考查原电池的设计方法,利用氧化还原反应分析是解题的关键,燃料电池电极反应式的书写要注意电解质的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 加入AgNO3溶液,有白色沉淀生成,证明含有Cl- | |
| B. | 加入BaCl2溶液,产生白色沉淀,证明有SO42- | |
| C. | 加入盐酸,放出能使澄清石灰水变浑浊的气体,证明有CO32- | |
| D. | 加浓NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝色的气体,证明有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
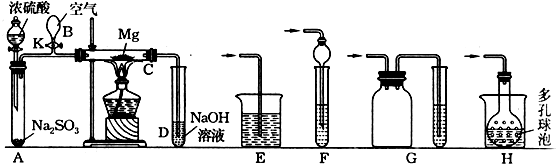
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(B2)=0.8mol/(L•s) | B. | V(A2)=0.4mol/(L•s) | C. | V(C)=0.6mol/(L•s) | D. | V(B2)=1.8mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨是指pH<7的酸性降水 | |
| B. | 淡水的密度小于海水的密度 | |
| C. | 蒸馏法是海水淡化的方法之一 | |
| D. | 融化的雪水中矿物质含量比深井水中的少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 31.3 g | B. | 27.9 g | C. | 25.6 g | D. | 19.8 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com