
| A. | 如图电解一段时间后溶液颜色变浅 | B. | 如图待镀铁制品与电源负极相连 | ||
| C. | 如图电子由b极流向a极 | D. | 如图阴极反应式:Ix-+(x-1)e-=xI- |
分析 A、惰性电极电解氯化铜即电解氯化铜本身;
B、在电镀池中,镀件金属应该做阴极,镀层金属做阳极;
C、电子由负极流向正极;
D、阴极得电子发生还原反应.
解答 解:A、装置①惰性电极电解氯化铜即电解氯化铜本身,所以氯化铜浓度越来越小,所以溶液颜色变浅,故A正确;
B、在电镀池中,镀件金属应该做阴极,镀层金属做阳极,所以待镀铁制品应做阴极,与电源负极相连,故B正确;
C、电子由负极流向正极,又氢氧燃料电池氢气为负极,氧气为正极,所以电子由a极流向b极,故C错误;
D、如图阴极Ix-得电子发生还原反应生成I-,反应式:Ix-+(x-1)e-=xI-,故D正确.
故选C.
点评 本题考查学生原电池和电解池的工作原理知识,注意把握电极的判断方法,注意平时知识的积累是解题的关键,难度中等.


科目:高中化学 来源: 题型:解答题
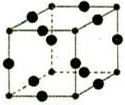 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体通入NaClO溶液中,若生成HClO,则可证明HClO是弱酸 | |
| B. | 高温下SiO2与碳酸盐反应,若生成CO2气体,则说明硅酸的酸性比碳酸强 | |
| C. | 向已配制的FeSO4溶液中加入2至3滴KSCN溶液,若溶液呈血红色,则说明可能有部分Fe2+被氧化为Fe3+ | |
| D. | 将铜片与浓硫酸混和共热,片刻后停止加热,冷却后再将溶液小心倒入盛有蒸馏水的烧杯中,若溶液呈蓝色,则说明铜能被浓硫酸氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1 | |
| B. | 由N2(g)+3H2(g)2NH3(g)△H=-92.4 kJ•mol-1热化学方程式可知,当反应中转移6NA(NA为阿伏加德罗常数的值)电子时,反应放出的热量等于92.4kJ | |
| C. | HCl和NaOH反应的中和热△H=-57.3kJ•mol-1,则H2SO4和KOH反应的中和热△H=-57.3kJ•mol-1 | |
| D. | 在101 kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=+571.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 压强/Mpa 体积分数/% 温服/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A. | 该反应的△S>0 | B. | 915℃,2.0 MPa时E的转化率为40% | ||
| C. | b<f | D. | K(1000℃)>K(810℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2,3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com