
【题目】电解尿素的碱性溶掖可以制取氢气,其装置如图所示(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列有关说法中不正确的是( ) 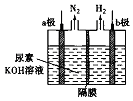
A.电解过穆中b极附近溶液碱性明显增强
B.溶液中的OH﹣逐渐向a极区附近移动
C.若在b极产生标准状况下224mL氢气,则消耗尿素2g
D.a极反应式为CO(NH2)2+8OH﹣﹣6e﹣═CO32﹣+N2↑+6H2O
【答案】C
【解析】解:A.该电池反应中,b极H元素化合价由+1价变为0价生成氢气,电极反应式为2H2O+2e﹣═H2↑+2OH﹣,所以b极附近溶液碱性明显增强,故A正确;
B.电解时,电解质溶液中阴离子向阳极移动,根据a极氮元素化合价由﹣3价变为0价失电子为阳极,所以氢氧根离子向a极移动,故B正确;
C.阴极b上水得电子生成氢气和氢氧根离子,电极反应式为2H2O+2e﹣═H2↑+2OH﹣,标况下224mL H2物质的量为0.01mol,转移电子0.02mol,a极为阳极,电极反应式为:CO(NH2)2+80H﹣﹣6e﹣═CO32﹣+N2↑+6H2O,消耗尿素0.2g,故C错误;
D.电解时a极为阳极,电极反应式为:CO(NH2)2+80H﹣﹣6e﹣═CO32﹣+N2↑+6H2O,故D正确;
故选:C.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】我国最近在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是

A. 该制氢工艺中光能最终转化为化学能
B. 该装置工作时,H+由b极区流向a极区
C. a极上发生的电极反应为Fe3++e-=Fe2+
D. a极区需不断补充含Fe3+和Fe2+的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+ 4B(g)![]() C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
A. vA=0.15mol/(L·min) B. vB=0.6 mol/(L·min)
C. vC=0.4 mol/(L·min) D. vD=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素③的原子结构示意图______;元素⑨形成的氢化物的电子式___________。
(3)表中元素④、⑨形成的氢化物的稳定性顺序为_____> (填化学式)。
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为_____> (填化学式)。
(5)表中元素③、④、⑥、⑦的原子半径大小为____> > > (填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。
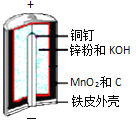
放电时总反应为:Zn + 2H2O + 2MnO2![]() Zn(OH)2 + 2MnOOH
Zn(OH)2 + 2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:
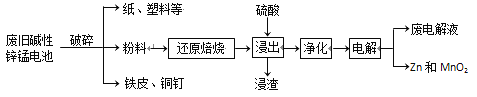
回答下列问题:
(1)MnOOH中,Mn元素的化合价为________。
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有________。
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入________(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。(离子浓度小于1×10-5mol·L-1即为沉淀完全)已知浸出液中Mn2+、Zn2+的浓度约为0.1 mol·L-1,根据下列数据计算调节pH的合
理范围是________至________。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“电解”时,阳极的电极反应式为_____。本工艺中应循环利用的物质是_____(填化学式)。
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为________。
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有________%的金属锌未参加反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成生物体化学元素的论述,正确的是
A. 组成生物体和组成无机自然界的化学元素中,碳元素的含量最多
B. 不同生物体内各种化学元素的含量比例基本相似
C. 组成生物体的化学元素在无机自然界都可以找到
D. 动物与植物所含的化学元素的种类差异很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期非金属元素甲~戊在元素周期表中的相对位置如下表所示:
甲 | 乙 | |
丙 | 丁 | 戊 |
下列判断正确的是( )
A.原子半径:丙<丁<戊
B.非金属性:甲>丙
C.氧化物的水化物:丙<丁<戊
D.最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃被酸性高锰酸钾溶液氧化的规律是,双键两端的基团=CH2变成CO2 , =CHR变成RCOOH, ![]() 变成
变成 ![]() ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
A.只有CH3COOH
B.CO2和 CH3COCH3
C.CO2和CH3CH2COOH
D.HCOOH和CH3CH2COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 78gNa2O2固体中含有的离子数之和为3NA
B. 标准状况下22.4LCl2通入足量水中,反应中转移的电子数为NA
C. 18gD2O所含有的质子数、电子数均为10NA
D. pH=1的醋酸溶液中含有的H+数目为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com