
【题目】已知常温下Ksp(AgCl)=1.6×10-10、Ksp(AgI)=2.0×10-16,下列说法中正确的是
A.含有大量Cl-的溶液中肯定不存在Ag+
B.AgI悬浊液中加入少量KI粉末,平衡AgI(s)![]() Ag+(aq)+I-(aq)向左移动,溶液中离子的总浓度会减小
Ag+(aq)+I-(aq)向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中逐渐加入KI固体至c(I-)=Ksp(AgI)/Ksp(AgCl)mol·L-1时,AgCl开始向AgI沉淀转化
D.向浓度均为0.01 mol·L-1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl-开始沉淀时,溶液中I-的浓度为1.25×10-8 mol·L-1
【答案】D
【解析】
试题A、根据溶解平衡可知,含有大量Cl-的溶液中一定存在Ag+,A错误;B、AgI悬浊液中加入少量KI粉末,平衡AgI(s)![]() Ag+(aq)+I-(aq)向左移动,但又引入了钾离子,所以溶液中离子的总浓度不会减小,B错误;C、AgCl悬浊液中逐渐加入KI固体至c(I-)=Ksp(AgI)/Ksp(AgCl)mol·L-1时,说明溶液中氯离子浓度是1mol/L,所以不能说明AgCl开始向AgI沉淀转化,C错误;D、向浓度均为0.01 mol·L-1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl-开始沉淀时,溶液中银离子浓度为1.6×10-8mol/L,所以溶液中I-的浓度为2.0×10-16÷1.6×10-8mol/L=1.25×10-8 mol·L-1,D正确,答案选D。
Ag+(aq)+I-(aq)向左移动,但又引入了钾离子,所以溶液中离子的总浓度不会减小,B错误;C、AgCl悬浊液中逐渐加入KI固体至c(I-)=Ksp(AgI)/Ksp(AgCl)mol·L-1时,说明溶液中氯离子浓度是1mol/L,所以不能说明AgCl开始向AgI沉淀转化,C错误;D、向浓度均为0.01 mol·L-1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl-开始沉淀时,溶液中银离子浓度为1.6×10-8mol/L,所以溶液中I-的浓度为2.0×10-16÷1.6×10-8mol/L=1.25×10-8 mol·L-1,D正确,答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COONa溶液和NaCN溶液,所得滴定曲线如图(忽略体积变化)。下列说法正确的是( )
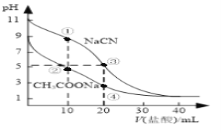
A. 溶液中阳离子的物质的量浓度之和:点②等于点③
B. 点①所示溶液中:c(CN-)+c(HCN)﹤2c(Cl-)
C. 点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)>c(CH3COOH)
D. 点④所示溶液中:c(Na+)+c(CH3COOH)+c(H+)>0.10mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知实验室制氯气的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,现用足量浓盐酸与8.7 g二氧化锰完全反应制取氯气(假设Cl2全部逸出)。求:
MnCl2+Cl2↑+2H2O,现用足量浓盐酸与8.7 g二氧化锰完全反应制取氯气(假设Cl2全部逸出)。求:
(1)产生多少升氯气(标准状况)?____________________
(2)把产生的氯气通入足量NaOH溶液中,假设氯气全部参加反应,可产生多少mol NaClO?____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用。下列说法正确的是
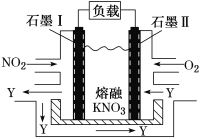
A. 放电时,NO3-向石墨Ⅱ电极迁移
B. 石墨Ⅱ附近发生的反应为NO+O2+e-===NO3-
C. 该电池总反应式为4NO2+O2===2N2O5
D. 当外电路通过4 mol e-时,负极上共产生2mol N2O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化示意图如图,其中“o”和“”代表不同元素的原子.下列关于此反应的说法不正确的是( )

A.该反应可表示为![]()
B.可能是PCl5的分解反应
C.反应过程中,一定伴随共价键的断裂与形成
D.该反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaClO2在水溶液中能发生水解。常温时,有1 mol/L的HClO2溶液和1mol/L的HBF4(氟硼酸)溶液起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积为V,所得曲线如图所示。下列说法错误的是
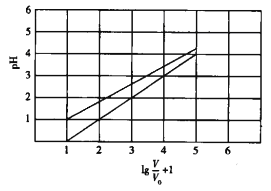
A. HClO2为弱酸,HBF4为强酸
B. 常温下HClO2的电高平衡常数的数量级为10—4
C. 在0≤pH≤5时,HBF4溶液满足pH=lg(V/V0)
D. 25℃时1L pH=2的HBF4溶液与100℃时1L pH=2的HBF4溶液消耗的NaOH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证同主族元素性质的递变规律。某小组用如图所示的装置进行实验(夹持仪器已略去,装置气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当装置B和装置C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当装置B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)浸有NaOH溶液的棉花的作用____________________________。
(2)装置A中发生的置换反应的化学方程式为___________________。
(3)装置B的溶液中NaBr完全被氧化,则消耗Cl2的物质的量为__________。
(4)为验证溴元素的非金属性强于碘元素,过程Ⅳ的操作和现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧生成CO2和H2O。将12.4 g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重10.8 g,再通过碱石灰,碱石灰增重了17.6 g。下列说法不正确的是
A. 该有机物的最简式为CH3O
B. 该有机物的分子式可能为CH3O
C. 该有机物的分子式一定为C2H6O2
D. 该有机物可能属于醇类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
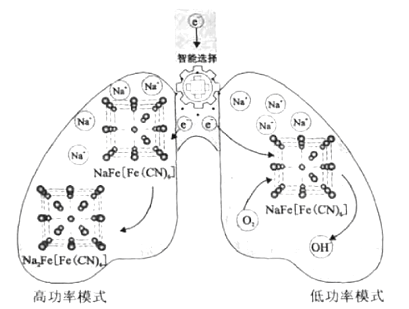
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com