
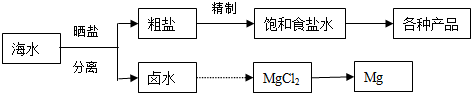
���� ��1���ٻ��ý�������ȡһ���ȡ��������εķ�����
���ɵ�ⷽ��ʽ�ɼ������������Ũ�ȣ��������PH��
�۸��������Ϣд����Ӧ����������ƽ���õ�ⷽ��ʽ��
��2���ٿ���þ���ӵ�ˮ�⣬һ�������Ƿ�ֹˮ��ķ�����
�ڰ�Ҫ�ͳɱ��ͼ�����Ⱦ�������������ÿɴﵽĿ�ģ�
�۴�����þ���۵㿼�ǣ�����þ�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ���
��� �⣺��1�������ƱȽϻ��ã���ȡʱֻ�ܲ��õ��ķ���������ʽΪ��2NaCl�����ڣ�$\frac{\underline{\;ͨ��\;}}{\;}$2Na+Cl2����
�ʴ�Ϊ��2NaCl�����ڣ� $\frac{\underline{\;ͨ��\;}}{\;}$2Na+Cl2����
�ڵ�ⱥ��ʳ��ˮ�������õ������������õ����������������ʵ���Ϊ��$\frac{0.112L}{22.4L/mol}$=0.005mol��
��2NaCl+2H2O $\frac{\underline{\;ͨ��\;}}{\;}$Cl2��+H2��+2NaOH ��֪��Cl2����H2����2NaOH����n��NaOH��=2n��Cl2��=2��0.005mol=0.01mol��c��NaOH��=$\frac{0.01mol}{0.1L}$=0.1mol/L������pH=13��
�ʴ�Ϊ��13��
�ۡ�84������ҺΪ����������Һ������Ȼ�����Һ��ȡ�������Ƶķ���ʽΪ��NaCl+H2O $\frac{\underline{\;ͨ��\;}}{\;}$NaClO+H2����
�ʴ�Ϊ��NaCl+H2O $\frac{\underline{\;ͨ��\;}}{\;}$NaClO+H2����
��2����MgCl2•6H2O��һ�������¼��ȵõ���ˮMgCl2����ֱ�Ӽ���MgCl2•6H2O����ٽ�Mg2+ˮ�⣬�ò�����ˮMgCl2����Mg2+ˮ������ԣ�����������Ȼ��������п�����Mg2+ˮ�⣬��һ������Ϊ��HCl�����У�Ŀ��������Mg2+ˮ�⣬
�ʴ�Ϊ���Ȼ��������У�����Mg2+ˮ�⣻
�ڵ�������Ȼ�þ�õ��������ж������ŷŴ����л���Ⱦ���������ѵ��õ����������������ϵõ��Ȼ��⣬���Ƶ�c����Ҫ�����ᣬ�����Ȼ�������������
Mg2+ˮ�⣬�������˳ɱ����ַ�ֹ����Ⱦ��
�ʴ�Ϊ��e����������Cl2������ȡHCl���壬����HCl����d����MgCl2ˮ�⣬���Ƶ�c�������������
������þ�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ����ʲ�ͬ���ͬѧ���뷨��
�ʴ�Ϊ����ͬ�⣬��ΪMgO�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ���
���� ���⿼���˴Ӻ�ˮ�л�ȡ��ѧ��Դ�����⣮�ڼ���PHʱ���ɸ��ݷ���ʽ���ϵʽ���м��㣬�ش�һ��������Ҫ��MgCl2�������֣��شͳɱ���Ҫ��ѭ�����á����ת���ʵȽǶȿ��ǣ���Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ�����ܣ�P��S | B�� | ��̬�⻯����ȶ��ԣ�CH4��NH3 | ||
| C�� | �縺�ԣ�CI��F | D�� | ��������ϼۣ�F��S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڳ��³�ѹ�£�11.2 ���������еķ�����Ϊ0.5NA | |
| B�� | 1 molFe��������Cl2��Ӧת�Ƶĵ�����Ϊ2NA | |
| C�� | ���³�ѹ�£�32 g O2��O3�Ļ����������ԭ����Ϊ2NA | |
| D�� | ��״���£�22.4 LSO3���е�ԭ����Ϊ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol FeI2������������Ӧʱת�Ƶĵ�����Ϊ2NA | |
| B�� | ��ϩ�ͻ�������ɵ�42g�����������ԭ�ӵĸ���Ϊ6NA | |
| C�� | 2 L 0.5 mol•L-1�������Һ�����������������ΪNA | |
| D�� | 1 mol Na2O2�����к���������Ϊ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
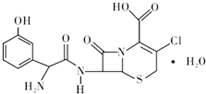 ͷ�߿������˹��ϳɵĵڶ����ڷ�ͷ�߾������أ���Ҫ�����ϡ��º�������Ⱦ���ж��ס�Ƥ���������Ⱦ��֢״����ṹ��ͼ��ʾ�����й���ͷ�߿����˵��������ǣ�������
ͷ�߿������˹��ϳɵĵڶ����ڷ�ͷ�߾������أ���Ҫ�����ϡ��º�������Ⱦ���ж��ס�Ƥ���������Ⱦ��֢״����ṹ��ͼ��ʾ�����й���ͷ�߿����˵��������ǣ�������| A�� | �����ʽ���Ա�ʾΪC15H16ClN3O6S | |
| B�� | �����ʾ������� | |
| C�� | 1 mol�û�������NaOH��Һ����ʱ����NaOH�����ʵ������Ϊ 4 mol | |
| D�� | ��������FeCl3��Һ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ʱ���ر䶼�뷴Ӧ���Է����йأ��ֶ����ܶ�������Ϊ�Է��Ե��о� | |
| B�� | -10���Һ̬ˮ�ͻ��Զ������Ϊ��̬����Ϊ���������Ĺ��� | |
| C�� | ������ʵ�������ǣ����̵��Է���ֻ�������жϹ��̵ķ�����ȷ�������Ƿ�һ���ᷢ�����̷��������� | |
| D�� | ���ȷ�Ӧ��������ϵ�������ͣ�������Է����е���������Щ���ȷ�ӦҲ�����Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | 20�� | 60�� | 100�� |
| Na2Cr2O7 | 73.2 | 82.0 | 91.4 |
| K2Cr2O7 | 13.1 | 50.5 | 96.2 |
| NaCl | 36 | 37 | 39 |
| KCl | 34 | 45.5 | 56.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���õ�ⱥ��MgCl2��Һ�ķ�����ý���þ | |
| B�� | ��ⷨ������ͭ���ô�ͭ����������ͭ������ | |
| C�� | �������Al2O3�Ʊ�������ʱ���������ʯʹAl2O3�����ۻ� | |
| D�� | �ȼҵ�е��ʳ��ˮʱ�������ӽ���Ĥ�ɷ�ֹ������NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com