
对于以下三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题。
(1)PCl5(g)PCl3(g)+Cl2(g)
再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率________,PCl5(g)的百分含量______。
(2)2HI(g)I2(g)+H2(g)
再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
(3)2NO2(g)N2O4(g)
再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
科目:高中化学 来源: 题型:
某校化学研究性学习小组的同学在学习了氨气的性质后讨论:既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列实验:
Ⅰ.制取氨气
(1)实验室常用加热氯化铵固体和氢氧化钙固体混合物的方法来制取氨气。写出实验室制取氨气的化学方程式:__________________________________。
(2)实验室还可向____________(填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为能否达到目的?________(填“能”或“否”),理由是_____________________________。
Ⅱ.实验探究
该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出)探究氨气的还原性(生成Cu和无污染的物质):
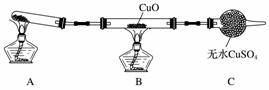
(1)写出氨气与CuO反应的化学方程式:________________________________________。
(2)为达到上述实验目的,预期的实验现象①________________________;②____________________________________________。
(3)该装置在设计上有一定的缺陷,为确保实验结果的准确性,对该装置的改进措施是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
固体A的化学式为NH5,它的所有原子的最外电子层结构都符合相应稀有气体的最外电子层结构,则下列有关说法不正确的是 ( )
A.1 mol NH5中含有5NA个NH键(NA表示阿伏加德罗常数的数值)
B.NH5中既有共价键又有离子键
C.NH5的电子式为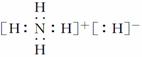
D.NH5与水反应的离子方程式为NH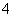 +H-+H2O===NH3·H2O+H2↑
+H-+H2O===NH3·H2O+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水法原理如下图所示,下列有关说法不正确的是 ( )。
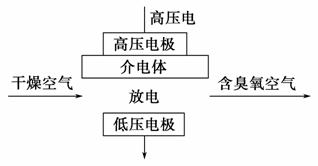
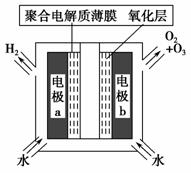
A.高压放电法,反应的原理为3O2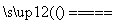 2O3
2O3
B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物
C.电解时,电极b周围发生的电极反应有3H2O-6e-===O3↑+6H+和
2H2O-4e-===O2↑+4H+
D.电解时,H+由电极a经聚合固体电解质膜流向电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
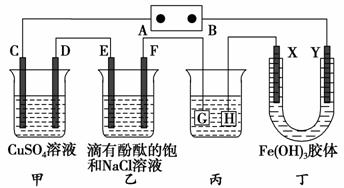
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
(1)B极是电源的________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明____________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______________。
(3)现用丙装置给铜件镀银,则H应该是________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______________________________________________________________
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将4.0 mol PCl3和2.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)。达到平衡时,PCl5为0.80 mol,如果此时移走2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.8 mol B.0.4 mol
C.小于0.4 mol D.大于0.4 mol,小于0.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
| 体积分数/%温度/℃压强/MPa | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1 000 | e | f | 83.0 |
①b<f ②915 ℃,2.0 MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1 000 ℃)>K(810 ℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个体积为2 L的密闭容器中,高温下发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)。其中CO2、CO的物质的量(mol)随时间(min)的变化关系如图所示。
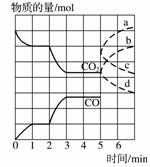
(1)反应在1 min时第一次达到平衡状态,固体的质量增加了3.2 g。用CO2的浓度变化表示的反应速率v(CO2)=__________。
(2)反应进行至2 min时,若升高温度,曲线发生的变化如图所示,3 min时再次达到平衡,则ΔH______0(填“>”、“<”或“=”)。
(3)5 min时再充入一定量的CO(g),平衡发生移动。下列说法正确的是________(填写字母)。
a.v正先增大后减小 b.v正先减小后增大
c.v逆先增大后减小 d.v逆先减小后增大
表示n(CO2)变化的曲线是__________(填写图中曲线的字母编号)。
(4)请用固态物质的有关物理量来说明该反应已经达到化学平衡状态:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去)。回答下列问题:
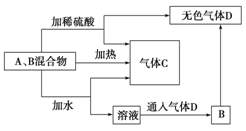
(1)写出A的电子式________________。
(2)①B加热产生D的化学方程式_________________________________________________________。
②B加稀硫酸产生D的离子方程式____________________________________________________。
(3)请用化学方程式表示A在潜水艇中的一种重要用途__________________________。
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com