
 �Դ�����Ⱦ��SO2��NOx�����о�������Ҫ�������壮��ش��������⣺
�Դ�����Ⱦ��SO2��NOx�����о�������Ҫ�������壮��ش��������⣺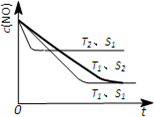 ��
�� ���� ��1������H2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-241.8kJ•mol-1
��C��s��+$\frac{1}{2}$O2��g��=CO��g����H=-110.5kJ•mol-1
�ɸ�˹���ɿ�֪����-�ٵõ�C��s��+H2O��g��=CO��g��+H2��g�����Դ˼��㷴Ӧ�Ȳ���д�Ȼ�ѧ����ʽ��
��2����2.0L�ܱ������ھ���5s��Ӧ�ﵽƽ�⣬���NOΪ1.6��10-3mol����
N2��g��+O2��g��?2NO��g��
��ʼ 0.8 0.2 0
ת��1.6��10-3 1.6��10-3 1.6��10-3��
�ٽ��v=$\frac{��c}{��t}$����NO�ķ�Ӧ���ʣ��ٽ������֮�ȵ��ڻ�ѧ������֮�ȼ��㵪���ķ�Ӧ���ʣ�ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
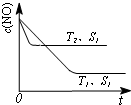
�������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��˵��ƽ��������У��¶�Խ������Խ�죻
��3���ٸ��ݵ���ƽ���ʱ�䣬�ж��¶ȸߵͣ��ٸ��ݲ�ͬ�¶��µ���ƽ��ʱNO��Ũ�ȸߵͣ��ж��¶ȶ�ƽ���Ӱ�죬�ݴ��жϷ�Ӧ��ЧӦ��
�ڴ����ı����S1��S2�������S1����ƽ���ʱ��ȴ���S2�̣�������Ӱ��ƽ���ƶ���ƽ��ʱNO��Ũ����ͬ���ݴ���ͼ��
��� �⣺��1����H2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-241.8kJ•mol-1
��C��s��+$\frac{1}{2}$O2��g��=CO��g����H=-110.5kJ•mol-1
�ɸ�˹���ɿ�֪����-�ٵõ�C��s��+H2O��g��=CO��g��+H2��g����H=-110.5kJ•mol-1-��-241.8kJ•mol-1��=+131.3kJ•mol-1��
�Ȼ�ѧ����ʽΪC��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ•mol-1��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ•mol-1��
��2����2.0L�ܱ������ھ���5s��Ӧ�ﵽƽ�⣬���NOΪ1.6��10-3mol��5s�ڸ÷�Ӧ��ƽ�����ʦͣ�NO��=$\frac{\frac{1.6��1{0}^{-3}mol}{2.0L}}{5s}$=1.6��10-4 mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ���ͣ�N2��=8.0��10-5 mol/��L•s�����ɻ�ѧ����ʽ��֪��Ӧ��ƽ�ⳣ������ʽΪK=$\frac{{c}^{2}��NO��}{c��{N}_{2}��c��{O}_{2}��}$��
�ʴ�Ϊ��$\frac{{c}^{2}��NO��}{c��{N}_{2}��c��{O}_{2}��}$��8.0��10-5 mol/��L•s����
�������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ�����¶����ߣ���Ӧ���ʼӿ죬ƽ�����ƣ�
�ʴ�Ϊ���¶����ߣ���Ӧ���ʼӿ죬ƽ�����ƣ�
��3�����¶�T2����ƽ���ʱ��̣���Ӧ���ʿ죬���¶�T2��T1���¶�Խ�ߣ�ƽ��ʱNO��Ũ��Խ�ߣ�˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ������
�ڴ����ı����S1��S2�������S1����ƽ���ʱ��ȴ���S2�̣�������Ӱ��ƽ���ƶ���ƽ��ʱNO��Ũ����ͬ����c��NO�� ��T1��S2�����´ﵽƽ������еı仯����Ϊ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼����ۺϣ��漰�Ȼ�ѧ����ʽ��д����ѧ��Ӧ���ʺ�Ӱ�컯ѧƽ������ء���ѧƽ��ͼ��ƽ�ⳣ���ȣ��ۺ��Խ�ǿ��ע�ػ�ѧ��Ӧ���ʼ���ѧƽ����ۺϿ��飬��3����ע����ݡ��ȹ���ƽ��ֵ��ԭ���ж��¶ȸߵͣ���ͼʱע���ƽ���ʱ����ƽ��ʱNO��Ũ�ȣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��У������ȤС���ڴ�����ˮ��Ʒʱ��������������Ϊ37%��Ũ���ᣨ�ܶ�Ϊ1��.19g/cm3�����Ƴ�250mL 0.1mol•L-1��������Һ��
��У������ȤС���ڴ�����ˮ��Ʒʱ��������������Ϊ37%��Ũ���ᣨ�ܶ�Ϊ1��.19g/cm3�����Ƴ�250mL 0.1mol•L-1��������Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ����B | ||
| C�� | �������ʹѹǿ��С | D�� | ����A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��ҺΪ���Һʱ��������ӦΪAl+3OH--3e-�TAl��OH��3�� | |
| B�� | ��NaCl��Һ��NaOH��ҺΪ���Һʱ��������Ӧ��ΪO2+2H2O+4e-�T4OH- | |
| C�� | ��NaOH��ҺΪ���Һʱ������ڹ��������е��Һ��pH���ֲ��� | |
| D�� | ��ع���ʱ������ͨ�����·���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0 | B�� | 32g | C�� | 38.4g | D�� | 48g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ��ϩ | C�� | һ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ����Ƿ�ɢϵ | |
| B�� | һ�ַ�ɢϵ��ֻ�з�ɢ�ʺͷ�ɢ���������� | |
| C�� | ��ɢ��һ����Һ�� | |
| D�� | ����ɢ�ʺͷ�ɢ����״̬������Һ���̣���9����Ϸ�ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+ Na+CO32- Cl- | B�� | K+��Al3+��Cl-��OH- | ||
| C�� | Fe3+��Al3+��SCN-��Cl- | D�� | Ag+ Al3+ NO3-H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com