
将反应4(NH4)2SO4=N2↑+6 NH3↑+3SO2↑+SO3↑+7H2O的产物气体通入BaCl2溶液,下列判断正确的是
A.无沉淀生成
B.肯定没有BaSO3生成
C.得到的沉淀是纯净物
D.得到的沉淀是BaSO4和BaSO3组成的混合物
D
【解析】
试题分析:根据题意知,将反应后的混合气体通入到BaCl2溶液中发生的反应为:
SO3+H2O+2NH3 =(NH4)2SO4;(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl;SO2+H2O+2NH3=(NH4)2SO3 ;(NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl;结合分解生成的气体物质的量可知,1mol三氧化硫转化为1mol硫酸铵消耗氨气2mol,剩余4mol氨气,4mol氨气会和2mol二氧化硫反应生成2mol亚硫酸铵,2mol亚硫酸铵对应得到2mol亚硫酸钡,剩余1mol二氧化硫和1mol亚硫酸钡、1mol水反应生成1mol亚硫酸氢钡,剩余1mol亚硫酸钡,最后得到沉淀为1mol硫酸钡,1mol亚硫酸钡,因此得到沉淀为BaSO3和BaSO4。选D。
考点:考查二氧化硫和三氧化硫的性质及相关计算。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:阅读理解
| (1-84a) |
| 18a |
| (1-84a) |
| 18a |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

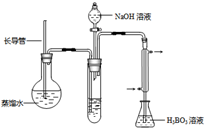 ④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| 加热 |
| ||
| 吹出 |
| ||
| 吸收 |

| 实验编号 | 样品和辅助试剂 | 消耗盐酸 体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+ NH4++NH2-
NH4++NH2- NH4++NH2-
NH4++NH2-查看答案和解析>>
科目:高中化学 来源: 题型:
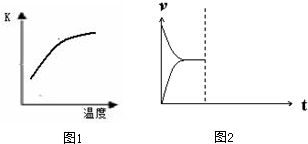
| C(H+) | C(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com