
| A. | 2.0mol/L | B. | 0.24mol/L | C. | 0.19 mol/L | D. | 3 mol/L |
分析 当碳酸钠滴入盐酸中时发生反应:CO32-+2H+═H2O+CO2↑,当盐酸滴入碳酸钠溶液时,发生反应:CO32-+H+═HCO3-、HCO3-+H+═H2O+CO2↑,不管是将前者加入后者中,还是将后者加入前者中,都有气体产生,说明n(HCl):n(Na2CO3)>1:1,但最终产生的气体体积不同,说明n(HCl):n(Na2CO3)<2:1,根据二者之间的关系式来分析解答.
解答 解:当碳酸钠滴入盐酸中时发生CO32-+2H+═H2O+CO2↑,当盐酸滴入碳酸钠溶液时,反应顺序为CO32-+H+═HCO3-、HCO3-+H+═H2O+CO2↑,不管是将前者加入后者中,还是将后者加入前者中,都有气体产生,说明n(HCl):n(Na2CO3)>1:1,但最终产生的气体体积不同,说明n(HCl):n(Na2CO3)<2:1,
所以1<n(HCl):n(Na2CO3)<2,n(Na2CO3)=0.20mol,则0.2mol<n(HCl)<0.4mol,盐酸的体积是200mL,所以$\frac{0.2mol}{0.1L}$<c(HCl)<$\frac{0.4mol}{0.1L}$,即2mol/L<c(HCl)<4mol/L,
故选D.
点评 本题考查化学方程式的有关计算,明确二者滴定顺序不同其反应方程式不同是解本题关键,再根据题意结合反应方程式进行计算,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋 | 红色很快褪为无色 | 随溶液pH减小,NaClO的氧化能力增强 |
| B | 向某氯化亚铁溶液中加入Na2O2粉末 | 出现红褐色沉淀 | 说明原氯化亚铁已氧化变质 |
| C | 苯酚和水的浊液中,加Na2CO3溶液 | 溶液变澄清 | 苯酚的酸性比碳酸强 |
| D | 向溶液X中加入NaHCO3粉末 | 产生无色气体 | 溶液X的溶质一定属于酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒容密闭容器中进行的反应3A(g)?B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大 | |
| B. | 对于可逆反应N2(g)+3H2(g)?2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 | |
| C. | 将FeCl3溶液和NaAlO2溶液相混,所得固体产物Fe(OH)3 | |
| D. | 反应NH3(g)+HCl(g)?NH4Cl(s)△H<O在任何条件下均能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+>I2>SO2>Cl2 | B. | Cl2>Fe3+>I2>SO2 | C. | I2>Cl2>Fe3+>SO2 | D. | Cl2>SO2>I2>Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解度(s) | B. | 物质的量浓度(c) | C. | 质量分数(w) | D. | 摩尔质量(M) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- | |
| B. | Mg(OH)2与盐酸的反应:OH-+H+═H2O | |
| C. | Al(OH)3沉淀中滴加盐酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
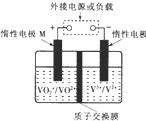 全钒液流储能电池利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,充电时,惰性电极M、N分别连接电源的正极和负极.电池工作原理如图所示,下列说法不正确的是( )
全钒液流储能电池利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,充电时,惰性电极M、N分别连接电源的正极和负极.电池工作原理如图所示,下列说法不正确的是( )| A. | 充电过程中,N电极附近酸性减弱 | |
| B. | 充电过程中,N电极上V3+被还原为V2+ | |
| C. | 放电过程中,H+由N电极向M电极移动 | |
| D. | 放电过程中,M电极反应为V02++2H++e-═V02++H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com