
【题目】下列叙述中,不能用平衡移动原理解释的是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成NH3的反应
C. 由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D. 黄绿色的氯水光照后颜色变浅
【答案】C
【解析】A.存在平衡2NO2(g)![]() N2O4(g),增大压强,混合气体的浓度增大,平衡体系颜色变深,该反应正反应为体积减小的反应,增大压强平衡正反应移动,二氧化氮的浓度又降低,颜色又变浅,由于移动的目的是减弱变化,而不是消除,故颜色仍比原来的颜色深,所以可以用平衡移动原理解释,故A不选;B.存在平衡N2 + 3H2
N2O4(g),增大压强,混合气体的浓度增大,平衡体系颜色变深,该反应正反应为体积减小的反应,增大压强平衡正反应移动,二氧化氮的浓度又降低,颜色又变浅,由于移动的目的是减弱变化,而不是消除,故颜色仍比原来的颜色深,所以可以用平衡移动原理解释,故A不选;B.存在平衡N2 + 3H2 ![]() 2NH3,正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成氨气,能用平衡移动原理解释,故B不选;C.存在平衡H2+I2(g)
2NH3,正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成氨气,能用平衡移动原理解释,故B不选;C.存在平衡H2+I2(g)![]() 2HI(g),该反应前后气体的体积不变,增大压强,平衡不移动,增大平衡体系的压强气体的体积减小,碘的浓度增大,颜色变深,不能用平衡移动原理解释,故C选;D.对氯水中的次氯酸受光照射会分解,次氯酸浓度减小,使得化学平衡Cl2+H2O
2HI(g),该反应前后气体的体积不变,增大压强,平衡不移动,增大平衡体系的压强气体的体积减小,碘的浓度增大,颜色变深,不能用平衡移动原理解释,故C选;D.对氯水中的次氯酸受光照射会分解,次氯酸浓度减小,使得化学平衡Cl2+H2O![]() HCl+HClO向右移动,能用平衡移动原理解释,故D不选;故选C。
HCl+HClO向右移动,能用平衡移动原理解释,故D不选;故选C。


科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
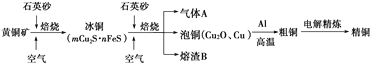
(1)气体A中的大气污染物可选用下列试剂中的________吸收.
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,检验溶液中还存在Fe2+的方法是________________________(注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为 ________________________________
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是________.
a.电能全部转化为化学能 b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动 d.利用阳极泥可回收Ag、Pt、Au等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.糖类、油脂、蛋白质都能发生水解反应
B.糖类、油脂、蛋白质都是由C、H、O三种元素组成的
C.糖类、油脂、蛋白质都是高分子化合物
D.油脂有油和脂肪之分,都属于酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
B. 电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C. 向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D. 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+
②Cr2O72﹣+6Fe2++14H+=2Cr3++6Fe3++7H2O,
下列有关说法错误的是( )
A.氧化性Cr2O72﹣>Fe3+>SO2
B.K2Cr2O7能将Na2SO3氧化成Na2SO4
C.每有1molK2Cr2O7参加反应,转移电子的数目为6NA
D.若6.72 L SO2(标准状况)参加反应,则最终消耗0.2molK2Cr2O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如右图所示。下列结论不正确的是( )

A. 反应开始4 min内温度对反应速率的影响比浓度大
B. 一段时间后,反应速率减小的原因是c(H+)减小
C. 反应在2~4 min内平均反应速率最大
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.06 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com