
 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.分析 (1)由图可知仪器的名称;
(2)分离四氯化碳和酒精的混合物,需要蒸馏,选酒精灯加热,冷却水下进上出;
(3)①转移液体需要玻璃棒引流;
②结合m=cVM计算;
③配制溶液的步骤为计算、称量、溶解、冷却、转移、定容、摇匀、装瓶;
(4)结合c=$\frac{n}{V}$及不当操作对n、V的影响判断误差.
解答 解:(1)由图可知仪器的名称为a.蒸馏烧瓶,b.冷凝管,c.容量瓶,e.锥形瓶,故答案为:蒸馏烧瓶;冷凝管;容量瓶;锥形瓶;
(2)分离四氯化碳和酒精的混合物,需要蒸馏,还缺少的仪器是酒精灯.冷凝水由g口通入,故答案为:酒精灯; g;
(3)①图中的错误是未用玻璃棒引流,故答案为:未用玻璃棒引流;
②用托盘天平所需称量NaOH的质量为0.5L×0.1mol/L×40g/mol=2.0g,故答案为:2.0;
③配制溶液的步骤为计算、称量、溶解、冷却、转移、定容、摇匀、装瓶,则配制时,其正确的操作顺序是B、C、A、F、E、D,故答案为:B、C、A、F、E、D;
(4)①用滤纸称量氢氧化钠,NaOH潮解,称量NaOH的质量偏小,n偏小,由c=$\frac{n}{V}$可知,浓度偏低,故答案为:偏低;
②定容时,若眼睛俯视刻度线,V偏小,由c=$\frac{n}{V}$可知,则所配制的溶液浓度将偏高,故答案为:偏高;
③未冷却到室温就注入容量瓶定容,V偏小,由c=$\frac{n}{V}$可知,则所配制的溶液浓度将偏高,故答案为:偏高;
④配好的溶液转入干净的试剂瓶时,不慎溅出部分溶液,对浓度无影响,故答案为:无影响.
点评 本题考查混合物分离提纯实验及溶液配制实验,为高频考点,把握仪器的使用、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意配制溶液的步骤及误差分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 向稀盐酸溶液中加入铁粉:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 甲 | 乙 | 丙 | |
| 容积 | 1L | 1L | 0.5L |
| 起始加入物质 | X:2mol,Y:1mol | Z:2mol | X:0.5mol,Y:0.25mol |
| 平衡时 | c(Z)=1.2mol•L-1 | c(Z)=1.2mol•L-1 |
| A. | T℃时该反应的平衡常数K为3.75 | |
| B. | 平衡时,X转化率:甲<丙 | |
| C. | 若乙是绝热容器,则平衡时,c(Z)>1.2mol•L-1 | |
| D. | 前2min内,丙容器中用X表示的平均反应速率v(X)=0.6mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
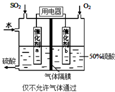 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
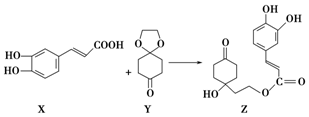
| A. | X的分子式为C9H8O4 | |
| B. | Y、Z中均含1个手性碳原子 | |
| C. | Z能发生加成反应、取代反应及消去反应 | |
| D. | 1 mol Z至多可与3 mol Br2发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com