
【题目】如图 ![]() 为直流电源,
为直流电源, ![]() 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, ![]() 为电镀槽,接通电路后发现
为电镀槽,接通电路后发现 ![]() 上的c点显红色,为实现铁上镀锌,接通
上的c点显红色,为实现铁上镀锌,接通 ![]() 后,使c、d两点短路.下列叙述正确的是 ( )
后,使c、d两点短路.下列叙述正确的是 ( )
A.a为直流电源的负极
B.c极发生的反应为2H++2e═﹣H2↑
C.f电极为锌板
D.e极发生还原反应
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:

下列说法不正确的是
A. b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B. 二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
C. 电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6gH2
D. 电解池a极的电极反应式为NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D反应中,表示该化学反应速率最快的是( )
A.v(A)=0.5mol/(Ls)
B.v(B)=0.3mol/(Ls)
C.v(C)=0.8mol/(Ls)
D.v(D)=1mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸过程中,SO2的催化氧化是主要反应之一.为了研究外界条件对该反应的影响,将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g)2SO3(g)△H<0,在一定条件下达到平衡,测得c(SO3)=0.040mol/L.
(1)判断该反应达到平衡状态的标志是(填字母)
A.SO2和SO3浓度相等
B.SO2百分含量保持不变
C.容器中气体的压强不变
D.SO3的生成速率与SO2的消耗速率相等
E.容器中混合气体的密度保持不变
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 . (填字母)
A.升高温度
B.降低温度
C.增大压强
D.减小压强
E.加入催化剂 G.移出氧气
(3)计算该条件下反应的平衡常数K= . SO2的平衡转化率为 .
(4)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 在气体单质分子中,一定含有σ键,可能含有π键
B. 烯烃比烷烃的化学性质活泼是由于烷烃中只含σ键而烯烃含有π键
C. 等电子体结构相似,化学性质相同
D. 共价键的方向性决定了原子在形成分子时相互结合的数量关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应:
2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=﹣266kJ/mol
O2(g)△H=﹣266kJ/mol
试回答:
(1)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为: .
(2)沼气是一种能源,它主要成分是CH4 . 0.5mol CH4完全燃烧生成CO2和液态水时,放出445kJ热量,则其燃烧的热化学方程式为: .
(3)SiH4是一种无色的气体,遇到空气能发生爆炸性自燃,生成SiO2(s)和H2O(l),已知室温下3.2gSiH4自燃放出热量79.2kJ,其热化学方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2NO2(g) ![]() N2O4(g),在一定条件下达到平衡,在温度不变时,欲使
N2O4(g),在一定条件下达到平衡,在温度不变时,欲使![]() 的比值增大,应采取的措施是
的比值增大,应采取的措施是
①体积不变,增加NO2的物质的量 ②体积不变,增加N2O4的物质的量
③使体积增大到原来的2倍 ④充入N2,保持压强不变
A. ①② B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
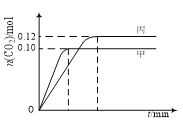
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的大
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com