
| A. | 升高温度(不考虑盐酸挥发) | B. | 改用10 mL 0.1 mol/L硝酸 | ||
| C. | 加入NaCl溶液 | D. | 滴入几滴硫酸铜溶液 |
分析 可以通过增大盐酸浓度、升高温度等方法来改变,但改变条件时不能加入和稀盐酸反应生成氢气的物质,以此解答该题.
解答 解:A.升高温度(不考虑盐酸挥发),增大活化分子百分数,化学反应速率增大,且不影响生成氢气总量,故A正确;
B.硝酸与铁反应不生成氢气,故B错误;
C.加NaCl溶液,氢离子浓度降低,反应速率减慢,故C错误;
D.滴入几滴硫酸铜溶液,Fe和铜离子发生置换反应生成Cu,Fe、Cu和稀盐酸构成原电池而加快反应速率,但生成氢气总量减小,故D错误.
故选A.
点评 本题考查化学反应速率影响因素,为高频考点,浓度、温度、催化剂、反应物接触面积、压强都是影响化学反应速率因素,注意这些外界条件的适用范围,注意硝酸的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
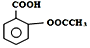 所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )
所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )| A. | 该化合物的分子式为C9H10O4 | |
| B. | 乙酰水杨酸的所有原子均在同一平面上 | |
| C. | 与乙酰水杨酸具有相同官能团,且苯环上只有两个取代基的芳香族同分异构体共有8种(不考虑立体异构) | |
| D. | 服用阿司匹林药量过大时,可出现精神错乱、惊厥甚至昏迷等水杨酸反应,可用小苏打溶液解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
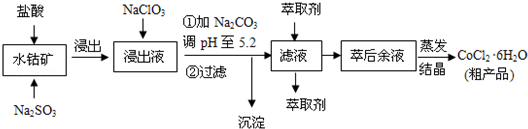
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl2-$?_{放电}^{充电}$2VCl3+Br-.
一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl2-$?_{放电}^{充电}$2VCl3+Br-.| A. | VCl2存储在正极储液罐内 | |
| B. | 放电时H+从负极区移至正极区 | |
| C. | 充电时电池的负极与电源的负极相连 | |
| D. | 充电时阳极反应为Br-+2Cl--2e-=BrCl2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁遇冷浓硝酸表面被钝化,可保护内部不被腐蚀 | |
| B. | 船底镶嵌锌块,锌做负极,以防止船体被腐蚀 | |
| C. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| D. | 电解精炼铜时以纯铜作阴极,粗铜做阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯与氯气 | B. | 丙烯与溴的CCl4溶液 | ||
| C. | 溴乙烷与氢氧化钠 | D. | 乙醇与浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
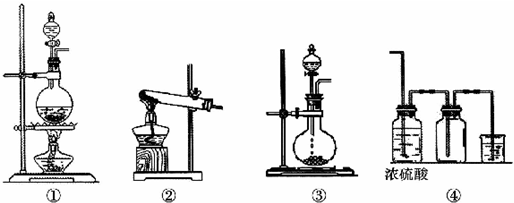
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com