

| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ•mol-1) | 436 | 247 | 432 |
分析 (1)右图是NO2和CO反应生成CO2和NO过程中能量变化示意图,反应物能量高于生成物能量,反应是放热反应,反应焓变=E1-E2,依据热化学方程式书写方法写出NO2和CO反应的热化学方程式;
(2)①根据△H=反应物总键能-生成物总键能计算;
②根据图象判断出abcd对应的各氢化物,根据焓变的大小书写热化学方程式;
(3)盖斯定律盖斯定律盖斯定律的含义是反应热是状态函数,与反应途径无关,根据目标方程式将已知的热化学方程式运用叠加的方法,得到目标方程式,反应热作相应的运算.
解答 解:(1)结构NO2和CO反应生成CO2和NO过程中能量变化示意图可知,反应物能量高于生成物能量,反应是放热反应,反应焓变=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol,标注物质聚集状态和对应焓变,写出NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ/mol,
故答案为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ/mol;
(2)①△H=436kJ/mol+243kJ/mol-2E(H-Cl)=-185kJ/mol,解得:E(H-Cl)=432kJ/mol,
故答案为:432kJ•mol-1;
②非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为:根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定,而能量越低越稳定,所以a、b、c、d依次为:H2Te、H2Se、H2S、H2O;
b为硒化氢的生成热数据,则硒化氢分解吸热,△H=-81kJ/mol,所以H2Se发生分解反应的热化学反应方程式为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol,
故答案为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol;
(3)①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ/mol,
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ/mol,
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+19kJ/mol,
根据盖斯定律(3×①-②-2×③)×$\frac{1}{6}$得:Fe(s)+CO(g)═Fe(s)+CO2(g)△H=$\frac{(-82kJ•mo{l}^{-1})×3-(-47kJ•mo{l}^{-1})-(+19kJ•mo{l}^{-1})×2}{6}$=-11KJ/mol,
故答案为:FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ/mol.
点评 本题考查了盖斯定律在热化学方程式中的应用,题目难度中等,明确盖斯定律的概念及含义为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
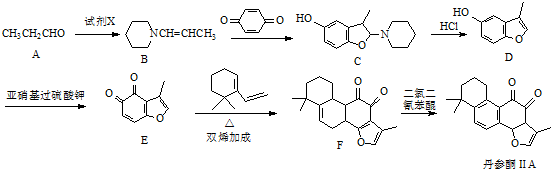
 .
. .
. 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据能量守恒定律,生成物总能量一定等于反应物总能量 | |
| B. | 放热反应的反应速率一定大于吸热反应的反应速率 | |
| C. | 表示中和热的热化学方程式:NaOH+HCl═NaCl+H2O△H=-57.3 kJ•mol-1 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40gNaOH溶于1L水所得的溶液 | |
| B. | 常温常压下,将22.4LHCl气体溶于水配成1L盐酸溶液 | |
| C. | 将23gNa溶于水并配成1L溶液 | |
| D. | 含K+为1 mol•L-1的K2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH相同的盐酸和醋酸加水稀释相同倍数后,pH前者大于后者 | |
| B. | 等质量的固态硫与硫蒸汽完全燃烧的反应热(△H),前者大于后者 | |
| C. | 温度、容积不变的密闭容器中2NO2?N2O4反应达到平衡,再充入N2O4气体,NO2的转化率前者大于后者 | |
| D. | 在相同条件下,2molH2和1molO2的能量的总和一定大于2mol水的能量的总和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com