
【题目】A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
(1)物质B、E和F的化学式为B、E、F;
(2)反应①的化学方程式为: , 其反应类型为 .
【答案】
(1)CuO;CO;Fe2O3
(2)C+2CuO ![]() 2Cu+CO2↑;置换反应
2Cu+CO2↑;置换反应
【解析】解:A~H都是初中化学中常见的物质,B为黑色固体,D为红色固体单质,A、B高温会生成C和D,所以D是铜,A、B有一种是氧化铜,A与C生成的E会与红色固体F反应,所以A是碳,B是氧化铜,C是二氧化碳,碳和二氧化碳高温会生成一氧化碳,所以E是一氧化碳,F是氧化铁,氧化铁和一氧化碳反应会生成G,所以G是铁,铁和硫酸铜等会生成硫酸亚铁和铜,所以H可以是硫酸铜,(1)根据上面的分析可知,B是CuO,E是CO,F是Fe2O3 ,
所以答案是:CuO;CO;Fe2O3;(2)反应①是碳和氧化铜在高温的条件下反应生成铜和二氧化碳,化学方程式为:C+2CuO ![]() 2Cu+CO2↑,该反应是单质和化合物生成单质和化合物的反应,属于置换反应.
2Cu+CO2↑,该反应是单质和化合物生成单质和化合物的反应,属于置换反应.
所以答案是:C+2CuO ![]() 2Cu+CO2↑;置换反应.
2Cu+CO2↑;置换反应.


科目:高中化学 来源: 题型:
【题目】如图是批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子。电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为:2CH3OH+3O2=2CO2+4H2O。下列说法中正确的是 ( )

A. 左边的电极为电池的负极,a处通入的是甲醇
B. 右边的电极为电池的负极,b处通入的是空气
C. 电池负极的反应式为:CH3OH+H2O+6e-=CO2+6H+
D. 电池的正极反应式为:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下按如图安装好实验装置,在锥形瓶内盛6.5 g锌粒(颗粒大小基本相同),通过分液漏斗加入40 mL 2.5 mol·L-1的硫酸溶液,将产生的H2收集在一个注射器中,用时10 s时恰好收集到气体的体积为50 mL(若折合成0 ℃、101 kPa条件下的H2体积为44.8 mL),在该温度下,下列说法不正确的是( )
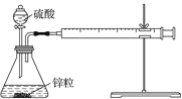
A. 可以通过测定锌粒减少质量来测定反应速率
B. 忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol·L-1·s-1
C. 忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应速率为0.01 mol·L-1·s-1
D. 用H2来表示10 s内该反应的速率为0. 000 2 mol·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了人类的可持续发展,我们应综合利用资源.保护环境,跟自然 和谐相处:
(1)科学家研制出有“自我修复能力”的塑料.塑料属于(选填“无机”、“合成”或“复合”)材料,为我们到来了方便,但废弃塑料处理不当会对环境造成不利的影响,人们把废弃塑料给环境带来的危害称为“”,发电厂是利用垃圾焚烧产生的转变为电能.
(2)发射“嫦娥三号”的长三甲火箭燃料是偏二甲肼(X),反应的化学方程式为:X+2N2O4=3N2+2CO2+4H2O,则X的化学式为
A.H2
B.CH4
C.C2H8N
D.C2H8N2
(3)2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”.关于水的知识有下列话题,请按要求填空: ①自来水生产过程中,可用方法除去水中不溶性杂质.
②在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作: 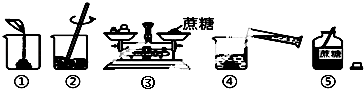
Ⅰ、如图操作中有错误的是(填序号).
Ⅱ、改正错误后,表示正确的操作顺序是(填序号).
A.⑤②①③④B.⑤①②③④C.⑤③②④①D.⑤③①④②
Ⅲ、保护水环境、珍爱水资源,是每个公民应尽的责任和义务.下列做法不利于保护水资源的是(填序号).
A.大量使用化肥农药 B.工业废水处理达标后再排放
C.使用含磷洗衣粉 D.生活污水直接排放.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O与D2O的pKw(p/Cw=-lgKw)与温度的关系如图所示,下列有关说法正确的是
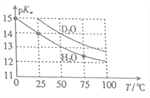
A. 常温下,向D2O中加入DCl,pKw变大
B. 25℃时,纯D2O的pH等于7
C. 25℃时,pH=7的液体一定是纯H2O
D. D2O的电离过程为吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是一种食品添加剂。实验室用如图所示装置制备Na2S2O5,实验步骤如下:

Ⅰ.向Na2CO3溶液中通入SO2至溶液pH为4.1,生成NaHSO3溶液;
Ⅱ.加入碳酸钠粉末至溶液PH为7~8;
Ⅲ.再通入SO2至溶液PH为4.1;
Ⅳ.从过饱和溶液中析出Na2S2O5晶体。
(1)制备焦亚硫酸钠总反应的化学方程式为___________________ 。
(2)Na2S2O5能与水发生化合反应,反应后所得的溶液显酸性。用电离方程式表示溶液显酸性的原因:____________________。
(3)利用碘量法可测定Na2S2O5产品中硫的含量。实验中必须使用的试剂有c1mol·L-1的标准碘溶液、c2 mol·L-1的标准Na2S2O3溶液、NaOH溶液、淀粉溶液。已知:Na2S2O5+2I2+3H2O=Na2SO4+H2SO4+4HI,2Na2S2O3+I2= Na2S2O6+2NaI。请补全实验方案:将一定量的Na2S2O5产品放入碘量瓶(带磨口塞的锥形瓶)中,加入—定体积的过量c1 mol L-1的标准碘溶液,充分反应后滴入NaOH溶液调节溶液pH至中性,____________________________。重复上述步骤2次,记录数据。
(4)含铬酸性废水中常含有+ 6价铬。利用Na2S2O5和FeSO4·7H2O分两个阶段先后处理含Cr2O72-的废水, Cr2O72-被还原为Cr3+,实验结果如图。

①0~40 min内用Cr2O72-表示的平均反应速率为____________mol L-1 min-1。
②60~80 min内Cr2O72-与Fe2+发生反应的离子方程式为_________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是M、N两种物质的溶解度曲线.t2℃时往盛有100g水的烧杯中先后加入ag M和ag N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.降温至t1℃,下列说法正确的是( ) 
A.t2℃时,得到M的饱和溶液
B.t2℃ 时,得到N的不饱和溶液
C.温度降低到t1℃时,得到M、N的不饱和溶液,且溶液中溶质的质量分数相等
D.温度降低到t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com