
一定条件下,分别对反应C(s)+CO2(g) 2CO(g)(正向吸热)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是 ( )
2CO(g)(正向吸热)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是 ( )
A.①②③④ B.①③④ C.①② D.①③
科目:高中化学 来源: 题型:
某同学对有关化学符号中数字的含义有如下理解,其中错误的是( )
A.Ca2+中的“2”表示一个钙离子带两个单位正电荷 B.2CO中的“2”表示两个一氧化碳分子
C.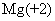 O中的“2”表示氧化镁中镁元素的化合价为+2价 D.CO2中的“2”表示一个氧分子由两个氧原子构成
O中的“2”表示氧化镁中镁元素的化合价为+2价 D.CO2中的“2”表示一个氧分子由两个氧原子构成
查看答案和解析>>
科目:高中化学 来源: 题型:
优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为:2Li+P2VP·nI2 = P2VP·(n-1)I2 +2LiI,则下列说法正确的( )
A. 正极的反应为:P2VP·nI2 + 2Li+ + 2e- = P2VP·(n-1)I2 + 2LiI
B.电池工作时,碘离子移向P2VP一极
C.聚2-乙烯吡啶的复合物与有机物性质相似,因此聚2-乙烯吡啶的复合物不会导电
D. 该电池所产生的电压低,使用寿命比较短
查看答案和解析>>
科目:高中化学 来源: 题型:
许多金属及它们的化合物在科学研究和工业生产中具有许多用途.回答下列有关问题:
(1)基态Ni核外电子排布式为________________, 第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________________;
(2) 已知CrO5中Cr为+6价,则CrO5的结构式为 。
已知CrO5中Cr为+6价,则CrO5的结构式为 。
 金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n ,与Ni(CO)n中配体
金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n ,与Ni(CO)n中配体
互为等电子体的离子的化学式为 (写出一个即可)。
 铜是第四周期最重要的过渡元素之一,其单质及化合物有广泛用途。已知CuH晶
铜是第四周期最重要的过渡元素之一,其单质及化合物有广泛用途。已知CuH晶
体结构单元如图所示。该化合物的的密度为ρg/cm3,阿伏加德罗常数的值为NA,则
该晶胞中Cu原子与H原子之间的最短距离为 cm(用含ρ和NA的式子表示)。

(3)另一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________,若该晶胞的边长为a pm,则合金的密度为_________ g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是
A、VA =0.5mol / (L.min) B、VB =0.3mol / (L.min)
C、VA =0.8mol / (L.min) D、VD = 1mol / (L.min)
查看答案和解析>>
科目:高中化学 来源: 题型:
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)  CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c) v(b)>v(d)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g) CO2(g)+H2(g) △H= -42kJ·mol-1
CO2(g)+H2(g) △H= -42kJ·mol-1
(1)在一定温度下,向一定体积的密闭容器中通入1molCO、2molH2O(g),反应达平衡时,测得放出的热量为28kJ,求CO的转化率为 ;
(2)该温度下,向该密闭容器中通入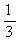 molCO2、
molCO2、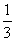 molH2,欲使反应达平衡时CO的体积分数与(1)相同,则还需满足的条件是 ;
molH2,欲使反应达平衡时CO的体积分数与(1)相同,则还需满足的条件是 ;
(3)该温度下,向该密闭容器中通入2molCO、3molH2O(g),反应达平衡时时,求H2O(g)的转化率 ;
(4)该温度下,向该密闭容器中通入1.5molCO、3molH2O(g),反应达平衡时,放出的热量为 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应A + B = C + D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是( )
A.△H <0、△S >0 B.△H >0、△S >0
C.△H <0、△S <0 D.△H >0、△S <0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com