
(12分)(1)用惰性电极电解饱和NaCl溶液,请写出:
① 阳极的电极反应为: ;
总反应离子方程式: 。
② 要使电解后的溶液恢复到和原溶液一样,则应加入一定量的 。
(2)用电解法精炼粗铜,电解液选用CuSO4溶液。请回答:
① 阳极的电极材料是 ,电极反应式是 ;
② 阴极电极的材料是 ,电极反应式是 。(杂质发生的电极反应不必写出)
(1)①2Cl--2e- = Cl2↑;2Cl- +2H2O 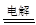 2OH- + H2↑
+ Cl2↑② HCl
2OH- + H2↑
+ Cl2↑② HCl
(2)①粗铜,Cu–2e- = Cu2+②精铜,Cu2++2e- = Cu
【解析】
试题分析:(1)用惰性电极电解饱和食盐水阳极反应式为2Cl--2e-= Cl2↑,阴极反应式为2H2O+2e-=H2↑+2OH-,总反应式为2Cl- +2H2O 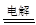 2OH- + H2↑
+ Cl2↑。
2OH- + H2↑
+ Cl2↑。
(2)粗铜电解精炼时粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解液。粗铜中比铜活泼的金属失电子溶解,比铜不活泼的金属形成阳极泥沉积到电解槽底部。阳极反应为Cu-2e-=Cu2+等,阴极反应为Cu2++2e-=Cu。
考点: 电解 铜的电解精炼
点评:粗铜电解精炼时粗铜作阳极,纯铜作阴极,电解液为硫酸铜溶液,粗铜中比铜活泼的金属失电子溶解,比铜不活泼的金属形成阳极泥沉积到电解槽底部,若长时间电解,需补充硫酸铜溶液。


科目:高中化学 来源: 题型:
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目:高中化学 来源:2012届陕西省西安中学高三第三次月考化学试卷(带解析) 题型:填空题
(10分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)用惰性电极电解硫酸铜溶液时,若某电解质量增加16g,则另一电极的电极方程式为___________;该电极可收集到标况下气体____________L。
(2) 的立体构型是________,其中S原子的杂化轨道类型是_______;
的立体构型是________,其中S原子的杂化轨道类型是_______;
(3))元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______。
查看答案和解析>>
科目:高中化学 来源:2013届天津市十二校高三第二次模拟联考化学试卷(带解析) 题型:填空题
钛(Ti)被称为继铁、铝之后的第三金属,也有人说21世纪是钛的世纪。钛在地壳中的含量并不少,但钛的冶炼技术还未获得突破,目前钛只用于尖端领域。
如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可大大提高资源利用率,减少环境污染。
请填写下列空白:
(1)用惰性电极电解2 L食盐水时,总反应的离子方程式_______________________________,当阴极上产生224 mL气体(标准状况)时,所得溶液的pH= (假设电解前后溶液体积不变,食盐水足量)。
(2)写出高温下钛铁矿经氯化得到四氯化钛的化学方程式 。(提示:FeTiO3中Ti为+4价)
(3)反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是____________________。
2MgCl4+Ti在Ar气氛中进行的理由是____________________。
(4)二甲醚是一种重要的清洁燃料,可以通过甲醇分子间脱水制得:
2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
T1 ℃时,在恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如下图所示。
①T1 ℃时,该反应的平衡常数为 ;
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)="0.4" mol/L、c(H2O)="0.6" mol/L、(CH3OCH3)="1.2" mol/L,此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”)。
(5)在上述产业链中,合成192吨甲醇理论上需额外补充H2__________吨 (不考虑生产过程中物质的任何损失)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省甘谷一中高二第二次月考化学试卷(带解析) 题型:填空题
(12分)(1)用惰性电极电解饱和NaCl溶液,请写出:
① 阳极的电极反应为: ;
总反应离子方程式: 。
② 要使电解后的溶液恢复到和原溶液一样,则应加入一定量的 。
(2)用电解法精炼粗铜,电解液选用CuSO4溶液。请回答:
① 阳极的电极材料是 ,电极反应式是 ;
② 阴极电极的材料是 ,电极反应式是 。(杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com