
| A. | 化学反应过程中形成新的化学键 | B. | 干冰升华 | ||
| C. | 加热才能发生的化学反应 | D. | 氧化钙与水反应 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 | |
| B. | 二氧化硅有良好的导电性,是制造光导纤维的主要材料 | |
| C. | 药皂中加入少量苯酚,可以起到杀菌消毒的作用 | |
| D. | 碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合物中铜和铁各0.15mol | |
| B. | 第一次剩余9.6g金属为铜和铁 | |
| C. | 稀硝酸的物质的量浓度为2.0mol/L | |
| D. | 向反应后的溶液中再加入该硝酸200mL,又得到标准状况下的NO体积小于2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO+CO═Fe+CO2 △H=-11kJ•mol-1 | |
| B. | FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-22kJ•mol-1 | |
| C. | FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ•mol-1 | |
| D. | FeO(s)+CO(g)═Fe(s)+CO2(g))△H=11kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
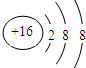 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3p2表示3p能级有两个轨道 | |
| B. | 1s22s12p1表示的是激发态原子的电子排布 | |
| C. | M能层中的原子轨道数目为3 | |
| D. | 处于同一轨道上的电子可以有多个,它的运动状态完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a-n=b+m | B. | a+m=b-n | ||
| C. | 氢化物为HnX或XHn | D. | 氧化物为YOm |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com