
 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:| 物质 T/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
分析 (1)由表中数据可知,C、NO、E、F的化学计量数之比为(3.000-2.960):(0.10-0.020):0.040:0.040=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2;
(2)计算各气体的平衡浓度,代入平衡常数表达式计算;
(3)反应C+2NO?N2+CO2是一个气体体积不变的反应,而反应物只有一种,故加入NO气体,建立的平衡和原平衡为等效平衡;
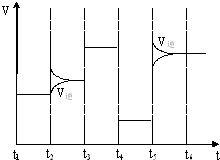
(4)t2、t3、t4、t5时改变某一种反应条件,所改变的条件均不同,可以判断每一时刻改变的条件.
解答 解:(1)由表中数据可知,C、NO、E、F的化学计量数之比为(3.000-2.960):(0.10-0.020):0.040:0.040=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2,且该反应为可逆反应,反应方程式为C+2NO?N2+CO2,故答案为:C+2NO?N2+CO2;
(2)平衡时c(NO)=$\frac{0.020mol}{2L}$=0.010mol/L,c(N2)=c(CO2)=$\frac{0.040mol}{2L}$=0.020mol/L,故T2℃时该反应的平衡常数为K2=$\frac{0.020×0.020}{0.01{0}^{2}}$=4,故答案为:4;
(3)反应C+2NO?N2+CO2是一个气体体积不变的反应,而反应物只有一种,故加入NO气体,建立的平衡和原平衡为等效平衡,原平衡中NO转化率为$\frac{0.10-0.020}{0.10}×100%$=80%,则达到新平衡时NO的转化率为80%,故答案为:80%;
(4)改变的条件均不同,t5时刻,正逆反应速率均增大,且逆反应速率大于正反应速率,故t5时刻改变条件为升温,所以正反应为放热反应,升温平衡逆向移动,T1<T2,该反应△H<0,故答案为:<;<.
点评 本题考查化学平衡图象、化学反应速率、影响化学平衡的因素,难度中等,是对知识的综合利用、注意基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
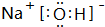 .
.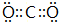 .属非极性分子(填分子极性).EC2其固体属原子晶体.
.属非极性分子(填分子极性).EC2其固体属原子晶体.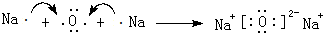 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
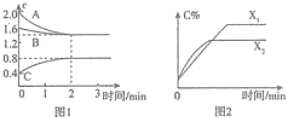
| A. | 0~2分钟、2~3分钟内用A浓度表示的平均反应速率:v(0~2)>v(2~3)>0 | |
| B. | 容器中发生的反应可表示为:3A(g)+B(g)?2C(g) | |
| C. | 若X表示温度,则生成C的反应是放热反应 | |
| D. | 若其他条件不变,仅减小起始时B的浓度,开始反应后C物质的浓度一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | 乙醇 | 汽油 | 加入CCl4萃取、分液 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | KNO3溶液 | KOH溶液 | 加入适量的CuSO4溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 铁在潮湿的空气中容易腐蚀 | |
| C. | 镀锌的铁制品比镀锡的铁制品耐用 | |
| D. | 常温下铝跟稀硫酸快速反应,跟浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
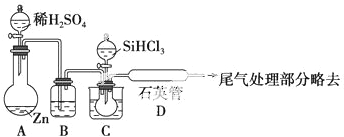
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com