
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.①→④→③→② | B.①→③→②→④ | C.①→③→④→② | D.①→②→③→④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol·L-1 | B.0.5 mol·L-1 | C.0.6 mol·L-1 | D.0.4 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝质轻,便于运输,储存,且安全 |
| B.铝燃烧时放出的热量大,且燃烧后的产物对环境的污染容易得到有效控制 |
| C.在地球上,铝矿资源丰富 |
| D.现代工业是利用电解铝的方法制取铝,这为把铝作为新能源奠定基础 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.三者的单质均为银白色固体 |
| B.三者都能与盐酸、稀硫酸反应 |
| C.AlCl3、FeCl3、CuCl2均可作净水剂 |
| D.制备Al 用电解法,制备Fe、Cu可用还原法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
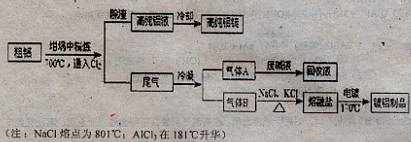
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
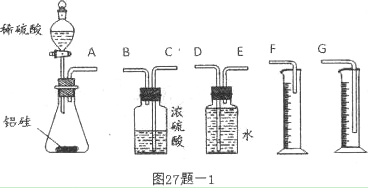
 _______________________________________________________________。
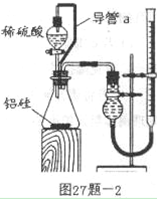
_______________________________________________________________。
 ___________________________
___________________________查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com