
【题目】中学化学常见物质A~I的转化关系如框图所示,其中A为化合物,B为常见金属单质,H的焰色反应为黄色,Y不使品红溶液褪色。(部分反应条件、溶剂及产物已略去)
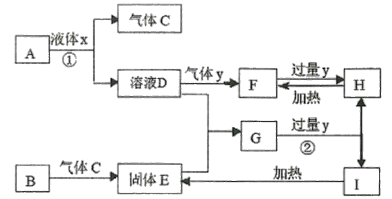
(1)反应①、②的离子方程式________________、__________。
(2)现有含0.10 mol H的溶液,要使其转化成含0.10 mol F的溶液,则:
①若只能加入0.050 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
②若只能加入0.10 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
【答案】2Na2O2+ 2H2O=4Na++ 4OH- +O2↑ AlO2- + 2H2O +CO2=Al(OH)3↓+ HCO3- Na2O或Na2O2 NaOH或Na
【解析】
由H的焰色反应为黄色,则含有钠元素,且能与F在加热与过量的y之间相互转化,则H为NaHCO3,F为Na2CO3,气体Y为CO2,溶液D为NaOH,化合物A能与液体x反应生成NaOH和气体C,那么A为Na2O2,液体x为H2O;因为B为金属单质,固体E为金属氧化物且能与氢氧化钠反应,则B为Al,E为Al2O3,G为NaAlO2,向NaAlO2通入二氧化碳产生Al(OH)3和NaHCO3,所以I为Al(OH)3,据此回答。
(1)反应①是Na2O2与H2O反应,所以离子反应方程式为2Na2O2+ 2H2O=4Na++ 4OH- +O2↑;反应②是向NaAlO2通入二氧化碳,所以离子反应方程式为:AlO2- + 2H2O +CO2=Al(OH)3↓+ HCO3-;
(2)由分析可知①Na2O或Na2O2,②NaOH或Na。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值。下列说法中正确的( )
A.11.7 g氯化钠晶体溶于水中Na+ 的数目为0.2 NA
B.19.6 g硫酸中含有的氧原子数为0.2 NA
C.标况下,1.12 L水中含有的原子数为0.15 NA
D.0.1mol·L-1的MgCl2溶液中,所含Cl- 的数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如下。
实验1 |
|
实验2 |
|
下列分析正确的是( )
A. 实验1中,白色沉淀a是Al2(CO3)3
B. 实验2中,白色沉淀b一定是Al2(OH)2(CO3)2
C. 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液
D. 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某实验小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
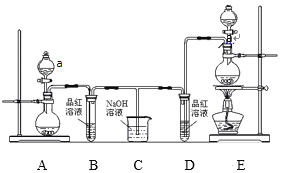
(1)仪器a的名称是 _________。
(2)利用图中E装置进行实验室制备Cl2的离子方程式是_________。
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是_______________。
(4)装置C的作用是_____________。
II.该小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。
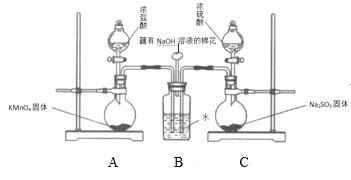
其中装置A制取氯气,装置C制取SO2:
(1)甲同学认为若SO2和Cl2反应,则应有Cl-生成,只要检验到生成的Cl-即可,甲取适量B中样品于试管中,向其中滴加少量_________溶液,有白色沉淀生成。
(2)乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得到正确结论。洗气瓶中盛有的试剂是_________。
(3)丙同学认为按乙同学的建议改进实验也不合理,理由是:___________。
(4)丙同学取BaCl2溶液于试管中,加入少量反应后B中的溶液,生成大量白色沉淀,得出正确结论:SO2与Cl2同时通入水中能相互发生反应,反应的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铁的还原剂CO是由焦炭和CO2反应而得。现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)![]() 2CO(g) △H=Q kJ/mol。图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是
2CO(g) △H=Q kJ/mol。图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是
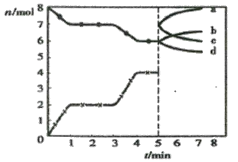
A.0~1min,v(CO)=1 mol/(L·min);1~3min时,v(CO)=v(CO2)
B.当容器内的压强不变时,反应一定达到平衡状态,且![]()
C.3min时温度由T1升高到T2,则Q>0,再达平衡时![]()
D.5min时再充入一定量的CO,a、d曲线分别表示n(CO)、n(CO2)的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过石油的裂化和裂解可以得到“工业三烯”即乙烯、丙烯、1,3-丁二烯等,最近有科学家发现正丁烷(![]() )脱氢或不完全氧化也可制得1,3-丁二烯(
)脱氢或不完全氧化也可制得1,3-丁二烯(![]() ),已知热化学方程式如下:
),已知热化学方程式如下:
①![]()
![]()
![]()
②![]() =
=![]()
![]()
③![]()
![]()
下列说法正确的是
A.由②可知,正丁烷(![]() )的燃烧热为
)的燃烧热为![]()
B.由①和②可知,同质量的正丁烷(![]() )转变为1,3-丁二烯(
)转变为1,3-丁二烯(![]() )所需要的能量相同
)所需要的能量相同
C. ![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)-
Ba(OH)2(aq)-![]() BaSO4(s)+H2O(l)
BaSO4(s)+H2O(l) ![]()
D.由①和②可推知:![]() =
=![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种物质存在如图转化关系,下列判断正确的是
![]()
A.若W是一种常见的金属单质,则X可能为![]()
B.若W为强碱,Y为白色难溶于水的固体,则工业上可以电解X的水溶液来制取其中所含的金属
C.若W固体俗称干冰,则Y晶体中的阴、阳离子个数比为1∶1
D.若W是![]() ,则Y一定是酸性氧化物
,则Y一定是酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将70g过氧化钠和氧化钠混合物与98g水充分反应,所得溶液恰好能被含硫酸98g的酸溶液中和,求:
(1)原混合物中过氧化钠和氧化钠的质量分别是多少?___
(2)所得氢氧化钠溶液的质量分数是多少?___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
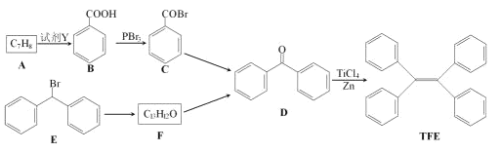
已知反应:![]() 。
。
回答下列问题:
(1)TFE的分子式为______________。
(2)A的名称为______________。
(3)A→B,E→F的反应类型分别为______________、______________。
(4)F→D的化学方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com