
分析 (1)某水溶液M中存在的分子有H2O、H2A,则H2A为弱酸;
(2)等体积混合生成Na2A,水解显碱性,离子水解以第一步为主;
A.离子水解以第一步为主,则离子浓度关系为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);
B.根据质子守恒:c(HA-)+2c(H2A)+c(H+)=c(OH-);
C.根据物料守恒分析可知:c(A2-)+c(HA-)+c(H2A)=$\frac{2mol•{L}^{-1}}{2}$=1mol•L-1;
D.根据电荷守恒:2c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+).
解答 解:(1)溶液中存在的分子有H2O、H2A,则H2A为弱酸,其电离方程式为:H2A?H++HA-、HA-?H++A2-,
故答案为:H2A?H++HA-、HA-?H++A2-;
(2)10mL 2mol•L-1NaHA溶液与10mL 2mol•L-1NaOH溶液混合生成Na2A,水解显碱性,pH>7,
A.离子水解以第一步为主,则离子浓度关系为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+),故A正确;
B.根据质子守恒:c(HA-)+2c(H2A)+c(H+)=c(OH-),故B错误;
C.根据物料守恒分析可知:c(A2-)+c(HA-)+c(H2A)=$\frac{2mol•{L}^{-1}}{2}$=1mol•L-1,故C正确;
D.根据电荷守恒:2c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+),故D错误;
故选AC.
故答案为:>;AC.
点评 本题考查较综合,涉及酸碱混合的定性分析、盐的水解等知识,把握溶液中的溶质的水解的趋势和守恒知识的应用即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 250C101KPa条件下,1摩尔任何气体的体积都是22.4升 | |
| B. | 标准状况下,体积是22.4升的物质,其物质的量一定是1摩尔 | |
| C. | 同温同压下两种气体,只要分子数相同,所占体积相同,质量也相同 | |
| D. | 同质量的O2和O3所含的氧原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②⑦ | C. | ①③ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
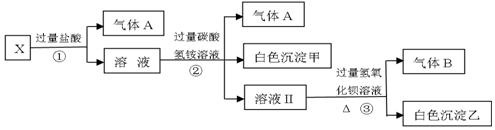
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸 | H2C2O4 | HF | H2CO3 | H3BO3 |
| 电离平衡常数Ka | Ka1=5.9×10-2 Ka2=6.4×10-5 | 未知 | Ka1=4.2×10-7 Ka2=5.6×10-11 | 5.8×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 19:8 | B. | 22:1 | C. | 13:8 | D. | 8:13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 非电解质 | 混合物 | 氧化物 | 弱电解质 | |
| A | Cu | 淀粉 | CuO | HClO |
| B | SO3 | 水玻璃 | Na2O•CaO•6SiO2 | H3PO4 |
| C | CH3CH2OH | KAl(SO4)2•12H2O | KClO3 | NH3•H2O |
| D | 葡萄糖 | 普通玻璃 | H2O | H2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com