
分析 (1)醋酸为弱酸,盐酸为一元强酸,硫酸为二元强酸,等pH时,醋酸浓度最大;
(2)物质的量浓度相同时,硫酸氢离子浓度最多,醋酸氢离子浓度最小;
(3)中和时,等浓度的三种酸,醋酸和盐酸的中和能力相同;
(4)体积和浓度相同的①、②、③三溶液,其物质的量相等,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积与酸的元数成反比;
(5)纯水中的c(H+)=c(OH-),某温度下,纯水中的c(H+)=2.0×10-7mol/L,则Kw=4.0×10-14,结合Kw计算.
解答 解:(1)pH相同溶液中氢离子浓度相同,醋酸是一元弱酸,硫酸是二元强酸、盐酸是一元强酸,假设氢离子浓度为1mol/L,则醋酸浓度大于1mol/L、盐酸浓度是1mol/L、硫酸浓度是0.5mol/L,所以其物质的量浓度的由大到小排列是 ①>②>③,故答案为:①>②>③;
(2)当它们的物质的量浓度相同时,假设都是1mol/L,醋酸中氢离子浓度小于1mol/L、硫酸中氢离子浓度是2mol/L、盐酸中氢离子浓度是1mol/L,氢离子浓度越大pH越小,所以其pH的由大到小排列是①>②>③,故答案为:①>②>③;
(3)中和等量氢氧化钠,消失同浓度酸的体积与酸电离出最终氢离子的浓度成反比,三种溶液浓度相等,硫酸是二元酸、醋酸和盐酸都是一元酸,所以最终电离出氢离子的浓度硫酸>醋酸=盐酸,所以消耗三种酸的体积大小顺序是①=②>③,故答案为:①=②>③;
(4)体积和浓度相同的①、②、③三溶液,其物质的量相等,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积与酸的元数成反比,硫酸是二元酸、醋酸和盐酸都是一元酸,所以需要烧碱溶液体积关系为 ①>②=$\frac{1}{2}$③,故答案为:①>②=$\frac{1}{2}$③;
(5)纯水中的c(H+)=c(OH-),某温度下,纯水中的c(H+)=2.0×10-7mol/L,则Kw=4.0×10-14,
若温度不变,滴入稀盐酸使c(H+)=5.0x10-6mol/L,则c(OH-)=$\frac{4×1{0}^{-14}}{5×1{0}^{-6}}$mol/L=8×10-9 mol/L,
故答案为:2×10-7;8×10-9.
点评 本题考查酸碱混合溶液定性判断,侧重考查学生分析、推断能力,明确一元酸、二元酸和碱的定量关系是解本题关键,题目难度中等.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:实验题
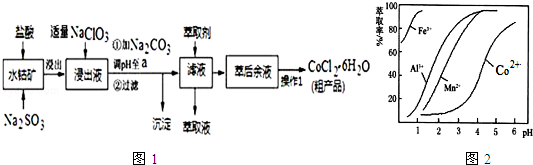
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蒸馏水中滴加稀H2SO4,c(H+)和KW都增大 | |
| B. | 在Na2S稀溶液中,c(OH-)+c(HS-)+2c(S2-)═c(H+)+c(Na+) | |
| C. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| D. | 等体积0.2mol/LHCl溶液与0.05mol/LBa(OH)2溶液混合后,溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ④②⑤①③ | D. | ⑤②④①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 v(NH3)=5 v(O2) | B. | 5 v(O2)=6 v(H2O) | C. | 5 v(NO)=4 v(O2) | D. | 3 v(H2O)=2 v(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | HClO4、H2SO4、H3PO4的酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
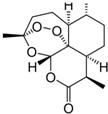 我国女药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )
我国女药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )| A. | 青蒿素的化学式为C15H22O5 | |
| B. | 青蒿素的同分异构体可能有芳香族化合物 | |
| C. | 青蒿素可与NaOH溶液发生水解反应 | |
| D. | 青蒿素可用蒸馏水从植物提取 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com