
| A�� | �����ȼ����Ϊ890.3KJ•mol-1�������ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| B�� | 500�桢30 MPa �£���0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��$?_{500��30MPa}^{����}$ 2NH3��g����H=-38.6 KJ•mol-1 | |
| C�� | ��֪1 gҺ̬�º�����Һ̬�������ⷴӦ���ɵ�����ˮ����ʱ�ų�20.05 kJ���������º������ⷴӦ���Ȼ�ѧ����ʽΪ�� N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.6 KJ•mol-1 | |
| D�� | CO��g����ȼ������283.0 KJ•mol-1����2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+283.0 KJ•mol-1 |
���� A��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ʱ�ų������������ɵ�ˮӦ��ΪҺ̬ˮ��
B��0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����ɵİ��������ʵ���С��1mol����ͬ�����µ�ͬһ���淴Ӧ�����淴Ӧ��Ӧ����ֵ��ȣ������෴��
C������n=$\frac{m}{M}$�����1g�µ����ʵ�����Ȼ��ɼ����1mol����ȫȼ�շų����������ٸ����Ȼ�ѧ����ʽ����дԭ�������
D��ȼ������ָ25��101KPʱ��1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų�����������Ӧ���뷽��ʽ�ļ����������ȣ�
��� �⣺A������ȼ������1mol������ȫȼ�������ȶ�������ų����������Ȼ�ѧ����ʽ��ˮ�����壬��ȷ���Ȼ�ѧ����ʽΪ������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890.3 kJ•mol-1����A����
B����ͬ�����µ�ͬһ���淴Ӧ�����淴Ӧ��Ӧ����ֵ��ȣ������෴��0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����ɵİ��������ʵ���С��1mol������2mol�����ֽ⣬���յ���������38.6kJ����B����
C.1 gҺ̬�µ����ʵ���Ϊ$\frac{1g}{32g/mol}$=$\frac{1}{32}$mol����1molҺ̬����ȫ��Ӧ�ų�������Ϊ20.05 kJ��$\frac{1mol}{\frac{1}{32}mol}$=641.6kJ���÷�Ӧ�Ļ�ѧ����ʽΪN2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.6 kJ•mol-1����C��ȷ��
D��ȼ������ָ25��101KPʱ��1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų�����������Ӧ���뷽��ʽ�ļ����������ȣ�CO��g����ȼ������-283.0kJ/mol����2CO��g��+O2��g��=2CO2��g����Ӧ�ġ�H=-2��283.0kJ/mol����2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+2��283.0 KJ•mol-1����D����
��ѡC��
���� ���⿼�����Ȼ�ѧ����ʽ����д��Ӧ�ã���Ŀ�Ѷ��еȣ���ȷȼ���ȡ��к��ȵĸ���Ϊ���ؼ���ע�������Ȼ�ѧ����ʽ����дԭ������������ѧ���ķ������������Ӧ��������


 �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д� �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
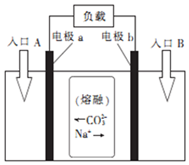 ��ֱ��úȼ�ϵ�ء��ܹ���ú�еĻ�ѧ�ܸ�Ч������ת��Ϊ���ܣ�������Na2CO3������ʵ�ֱ��úȼ�ϵ�صĹ���ԭ����ͼ�������й�˵����ȷ���ǣ�������
��ֱ��úȼ�ϵ�ء��ܹ���ú�еĻ�ѧ�ܸ�Ч������ת��Ϊ���ܣ�������Na2CO3������ʵ�ֱ��úȼ�ϵ�صĹ���ԭ����ͼ�������й�˵����ȷ���ǣ�������| A�� | �õ�ص��ܷ�ӦΪC+O2�TCO2 | |
| B�� | úֱ��ȼ�շ����ֱ��úȼ�ϵ�ط�������������ʸ� | |
| C�� | ���뷴Ӧ�ҵ�ú�����ɷ�ĩ״�Է�Ӧ���ʺ��Ⱦ���Ӱ�� | |
| D�� | �����ɵ缫b�ص�������缫a�����A���������Ϊú�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ijУ��ѧ��ȤС���ͬѧ����ɿα��Ҵ�����ȩ��ʵ��Ľ���ʵ�鷽������ͼ��������˳���������ʵ�������
ijУ��ѧ��ȤС���ͬѧ����ɿα��Ҵ�����ȩ��ʵ��Ľ���ʵ�鷽������ͼ��������˳���������ʵ�������| ʵ����� ʵ����� | ������Һ��S/mL | ��ȩ����/�� | �¶�/�� | ��Ӧ���Һ��pHֵ | ����������ʱ��/min |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
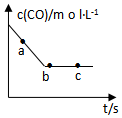 �����ŷŵ�β��Ϊ������ȾԴ֮һ��Ŀǰ�����������»�ѧԭ�����β����
�����ŷŵ�β��Ϊ������ȾԴ֮һ��Ŀǰ�����������»�ѧԭ�����β���� ��
��| ʵ���� | ʵ��Ŀ�� | T/�� | NO��ʼŨ�� mol/L | CO��ʼŨ�� mol/L | ͬ�ִ����ıȱ���� m2/g | ��ƽ��ʱ���õ�ʱ��min |
| �� | ����ʵ�� | 280 | 6.50��10-3 | 4.00��10-3 | 80 | t |
| �� | 280 | 6.50��10-3 | 4.00��10-3 | 120 | 0.5t | |
| �� | 360 | 6.50��10-3 | 4.00��10-3 | 80 | 0.2t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
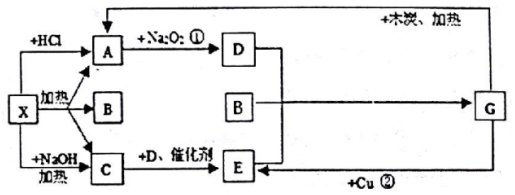
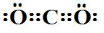 ��G�Ļ�ѧʽΪHNO3��
��G�Ļ�ѧʽΪHNO3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ̼Ԫ���γɵĵ��ʾ���ƽ���״�ṹ��ͬһ���е�ԭ�ӹ������������������Σ��˵������۴��ļ�����ã��γ�ij����ͭɫ�����ʣ����е�Ԫ�ؼ��á���ʾ����ԭ�ӷֲ���ͼ��ʾ�������ʵĻ�ѧʽΪKC8��
̼Ԫ���γɵĵ��ʾ���ƽ���״�ṹ��ͬһ���е�ԭ�ӹ������������������Σ��˵������۴��ļ�����ã��γ�ij����ͭɫ�����ʣ����е�Ԫ�ؼ��á���ʾ����ԭ�ӷֲ���ͼ��ʾ�������ʵĻ�ѧʽΪKC8���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
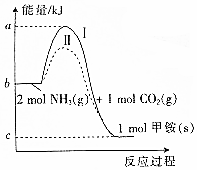 ��������泥�NH2COONH4����Ƽ�泥���CO2��NH3�����ص��м�������CO2��NH3��Ӧ���ɼ�淋������仯��ͼ��ʾ��
��������泥�NH2COONH4����Ƽ�泥���CO2��NH3�����ص��м�������CO2��NH3��Ӧ���ɼ�淋������仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2O | B�� | CF2=CF2 | C�� | CCl2F2 | D�� | SF6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com