
【题目】利用如图所示装置进行下列实验,将X溶液逐滴加入固体Y中,装置B的试管中的现象不正确的是( )
选项 | X溶液 | 固体Y | Z溶液 | 现象 |
|
A | 浓硫酸 | 亚硫酸氢钠 | 品红试液 | 品红褪色 | |
B | 浓氨水 | CaO | 紫色石蕊试液 | 溶液变红 | |
C | 盐酸 | 石灰石 | 硅酸钠溶液 | 出现白色沉淀 | |
D | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 |
科目:高中化学 来源: 题型:
【题目】

(1)写出图中仪器a的名称:_______________。
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为_____________,发生和收集装置为____________(填字母)。
(3)实验室用石灰石和稀盐酸反应智取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的______________端口(填“①”或“②”)通入,F中发生的化学反应方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)为白色粉末,微溶于水。常用作有机合成催化剂,并用于颜料、防腐等工业。实验室可采用亚硫酸钠还原氯化铜的方法制备氯化亚铜,主要流程如图所示:
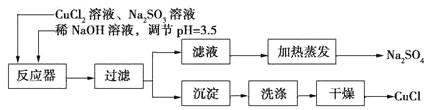
(1)上述方法制备氯化亚铜的化学方程式为_________________。
(2)下图是加热蒸发滤液,回收Na2SO4的装置。装置图中存在一处严重错误,该错误是_____________。

(3)洗涤产品氯化亚铜沉淀的试剂是____________,检验沉淀是否洗涤干净的方法是_______________。
(4)CuCl的盐酸溶液能吸收一氧化碳而生成氯化羰基亚铜[Cu2Cl2(CO)2·2H2O]。下图是用CO(含有CO2杂质)还原CuO并验证其氧化产物的实验装置图。
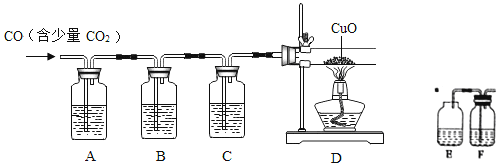
装置A中盛装的是饱和NaOH溶液,该装置的作用是______________,装置B盛有澄清的石灰水,其中装置B的作用是_____________,盛装CuCl的盐酸溶液的装置是__________(选填装置中提供的装置字母代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO![]() 、NO
、NO![]()
B.无色溶液中可能大量存在Al3+、NH![]() 、Cl-、S2-
、Cl-、S2-
C.1.0 mol·L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO![]()
D.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合时,其溶质的质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是( )
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成生物体的化学元素的说法,不正确的是
A. 细胞中常见的化学元素有20多种
B. 组成生物体的化学元素在无机环境中都可以找到
C. C是组成细胞的最基本的元素,因为C元素含量最多
D. 组成细胞的化学元素主要以化合物的形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 向某溶液中滴加KSCN 溶液,溶液呈血红色,证明存在Fe3+
B. 氢氧化钠溶液保存在带橡皮塞的试剂瓶中
C. 漂白粉常作环境消毒剂
D. 工业上用电解饱和食盐水来制取金属钠。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
①混合气体的平均摩尔质量是___________________。
②混合气体中所含碳原子的物质的量是_____________________。
③CO2和CO的体积之比是_______________________。
(2)标准状况下有①0.112 L水 ②0.5NA个HCl分子③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol He 所含原子个数从大到小的顺序为__________________。
(3)将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是_______________。(用含c1 和c2的代数式表示)
(4)某温度时,一定量的元素A的气态氢化物AH3,在恒温密闭容器中分解为两种气体单质,此时压强增加了75%,则AH3分解反应的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A.降低温度 B.加入适量的水
C.加入少量CuSO4溶液 D.加入浓度较大的盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com