
【题目】燃煤及工业废气中的SO2是形成酸雨的主要原因,消除SO2是减少酸雨形成的有效方法。完成下列问题:
(1)已知:4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=﹣3412.0kJmol﹣1
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣25.0 kJmol﹣1
2C(s)+O2(g)═2CO(g)△H=﹣221.0 kJmol﹣1
则2FeS2(s)+7O2(g)+3C(s)═2Fe(s)+3CO2(g)+4SO2(g)△H=_____kJmol﹣1。
(2)碱性NaClO2溶液脱硫法
SO2与碱性NaClO2溶液反应的离子方程式为2SO2+ClO2﹣+4OH﹣2SO42﹣+C1﹣+2H2O,已知pc=﹣lgc(SO2)。在刚性容器中,将含SO2的废气通入碱性NaClO2溶液中,测得pc与温度的关系如图所示。
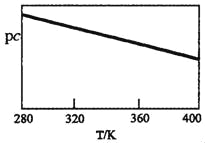
由图分析可知,该脱硫反应是_____反应(填“放热”或“吸热”);若温度不变,增大压强,该脱硫反应的平衡常数K_____(填“增大”、“减小”或“不变”)。
(3)燃料细菌脱硫法
①含FeS2的燃煤可用氧化亚铁硫杆菌(T.f)、氧化亚铁微螺菌(L.f)、氧化硫硫杆菌(T.t)进行脱硫,其脱硫过程如图所示:
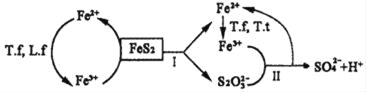
已知:脱硫总反应为:FeS2+14Fe3++8H2O═2SO42﹣+15Fe2++16H+,
Ⅰ反应的化学方程式为:FeS2+6Fe3++3H2O═S2O32﹣+7Fe2++6H+;
写出Ⅱ反应的化学方程式_____。
②在上述脱硫反应中,氧化亚铁硫杆菌(T.f)与Fe3+的形成过程可视为下图所示的原电池:

该细胞膜为_____(填“阳离子交换膜”或“阴离子交换膜”)。该电池的正极电极反应式为_____。该方法在高温下脱硫效率大大降低,原因是_____。
【答案】﹣2062.5 放热 不变 8Fe3++S2O32﹣+5H2O═2SO42﹣+8Fe2++10H+ 阳离子交换膜 O2+4H++4e﹣=2H2O 温度过高蛋白质发生变性,细菌失去催化能力 。
【解析】
(1)盖斯定律计算,利用同向相加、异向相减的原则;
(2)由图分析可知,升温平衡向吸热方向移动可知,对于平衡常数,如果是放热反应,随着温度上升,平衡常数减小;如果是吸热反应,随着温度上升,平衡常数上升;温度不变,K不变;
(3)①观察图像可知:反应Ⅱ是Fe3+和S2O32﹣反应生成亚铁离子和硫酸根离子,利用得失电子数相等、电荷守恒、原子守恒写出离子方程式;
②在脱硫反应中,氧化亚铁硫杆菌(T.f)与Fe3+的形成过程为如图所示的原电池反应,亚铁离子被氧化发生氧化反应在原电池负极反应,正极是氧气在酸性溶液中生成水,正极消耗氢离子,确定细胞膜为阳离子交换膜;温度过高蛋白质发生变性,细菌失去催化能力;
(1)已知:①4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=﹣3412.0kJmol﹣1
②Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=﹣25.0 kJmol﹣1
③2C(s)+O2(g)=2CO(g)△H=﹣221.0 kJmol﹣1
盖斯定律①×1/2+②+③×3/2计算 2FeS2(s)+7O2(g)+3C(s)=2Fe(s)+3CO2(g)+4SO2(g)△H=﹣2062.5KJ/mol;
答案:﹣2062.5。
(2)已知pc=﹣lgc(SO2),pc与温度的关系分析,温度越高Pc越小,则二氧化硫浓度增大,逆反应为吸热反应,正反应为放热反应,平衡常数只随温度变化,若温度不变,增大压强,该脱硫反应的平衡常数K不变;
答案:放热;不变。
(3)①反应Ⅱ是Fe3+和S2O32﹣反应生成亚铁离子和硫酸根离子,反应的离子方程式:8Fe3++S2O32﹣+5H2O═2SO42﹣+8Fe2++10H+;
答案:8Fe3++S2O32﹣+5H2O═2SO42﹣+8Fe2++10H+。
②脱硫反应中,氧化亚铁硫杆菌(T.f)与Fe3+的形成过程为如图所示的原电池反应,亚铁离子被氧化发生氧化反应在原电池负极反应,正极是氧气在酸性溶液中生成水,电极反应:O2+4H++4e﹣=2H2O,正极消耗氢离子,该细胞膜为阳离子交换膜,该方法在高温下脱硫效率大大降低,原因是:温度过高蛋白质发生变性,细菌失去催化能力;
答案:阳离子交换膜;O2+4H++4e﹣=2H2O;温度过高蛋白质发生变性,细菌失去催化能力。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:


(1)酸浸后加入H2O2的目的是______,调pH的最适宜范围为______。
(2)调pH过程中加入的试剂最好是_________。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是______。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式________________。
(4)称取所制备的CuCl样品0.2500g置于一定量的FeCl3溶液中,待样品完全溶解后加水20 mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数_______________。
(5)在一定条件下用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol·L-1的醋酸与b mol·L-1 Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=_________(用含a和b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家设计了一种可以循环利用人体呼出的CO2并提供O2的装置,总反应方程式为2CO2=2CO+O2.下列说法正确的是( )

A. 由图分析N电极为正极
B. OH﹣通过离子交换膜迁向左室
C. 阴极的电极反应为CO2+H2O+2e﹣=CO+2OH﹣
D. 反应完毕,该装置中电解质溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. 体系压强不再变化 D. 2v逆(X)=v正(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K、1.01×105Pa,O2、S、Se、Te分别与H2化合的反应热数据如图所示。写出Se与H2化合的热化学反应方程式正确的是

A. Se(s)+ H2(g) = H2Se(g) ΔH=-242kJ·mol-1
B. Se(s)+ H2(g) = H2Se(g) ΔH=-20kJ·mol-1
C. Se(g)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
D. Se(s)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中的平衡浓度与pH的关系如图所示(25℃):

③此实验条件下Mn2+开始沉淀的pH为7.54;离子浓度≤10-5mol·L-1时,离子沉淀完全。
请回答:
(1)传统工艺处理高硫锰矿时,不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为___________。
(2)“氧化”时,发生反应的离子方程式为_________________________________。若省略“氧化”步骤,造成的后果是_________________________________。
(3)“中和除杂”时,生成沉淀的主要成分为______________________(填化学式)。
(4)“氟化除杂”时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于___________。(已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12)
(5)“碳化结晶”时,发生反应的离子方程式为______________________。
(6)“系列操作”指___________、过滤、洗涤、干燥
(7)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 4.6gC2H5OH与6.0gCH3COOH反应,生成的 CH3COOC2H3分子数目为0.1NA
B. 5.6gFe与足量水蒸气完全反应,转移的电子数目为0.2NA
C. 32gO2和O3的混合物中含有的氧原子数目为2NA
D. 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下四种气体:
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
(1)质量由大到小的顺序为____________。
(2)气体密度由大到小的顺序为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中滴加另一种溶液或通入某种气体时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
A.盐酸中逐滴加入食盐溶液
B.醋酸中逐滴加入氢氧化钠溶液
C.饱和石灰水中不断通入CO2
D.醋酸中逐滴加入氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com