
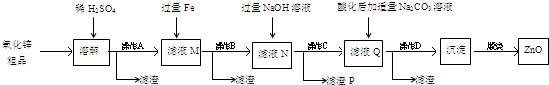
���� �Ʊ���������п����Ϊ������п��Ʒ�������������CuO��SiO2�����ʣ��м���ϡ���ᣬ����п���������������ͭ��ϡ���ᷴӦ���������費��Ӧ��ͨ�����˲���������������裬��Һ�к��������ӡ��������ӡ�п���ӡ�ͭ���ӣ�����ҺM����������ۣ�ͭ���ӱ��û���ͭ���ʣ�ͨ�����˵õ�����ҺN�к����������ӡ�п���ӣ�����ҺN�м�������������ƣ���Ӧ��������������������������������ҺQ�к���AlO2-���ữ��ҺQ���������̼������Һ�õ�����ZnCO3•2Zn��OH��2•H2O���������յõ�ZnO��
��1�����ݱ�������¶ȵȶԷ�Ӧ���ʵ�Ӱ����⣬����AΪ���ˣ����ݹ��˲�������д����ȱ�ٵ��������ƣ�
��2������ͭ���ӡ������ӡ������Ӷ��ܷ���������ԭ��Ӧ������Ԫ���غ�͵���غ���д��ѧ����ʽ��
��3��������Ϣ�жϷ�Ӧ���Ӧ������Ȼ��д����Ӧ�Ļ�ѧ����ʽ��
��4�����ݡ�ZnCO3•2Zn��OH��2•H2O�������ա���450��500���½��У����ջ��ZnO����֪��Ӧ���Ӧ�����������Ȼ��д����Ӧ�Ļ�ѧ����ʽ��
��5�����ݵ����غ��ҳ���ϵʽ��Ȼ����ݸ�����ص����ʵ���������������ӵ����ʵ������ٸ���c=$\frac{n}{V}$�������ҺN��Fe2+��Ũ�ȣ�
��� �⣺����ͼʾ��֪���Ʊ�����Ϊ������п��Ʒ�������������CuO��SiO2�����ʣ��м���ϡ���ᣬ����п���������������ͭ��ϡ���ᷴӦ���������費��Ӧ��ͨ�����˲���������������裬��Һ�к��������ӡ��������ӡ�п���ӡ�ͭ���ӣ�����ҺM����������ۣ�ͭ���ӱ��û���ͭ���ʣ�ͨ�����˵õ�����ҺN�к����������ӡ�п���ӣ�����ҺN�м�������������ƣ���Ӧ��������������������������������ҺQ�к���AlO2-���ữ��ҺQ���������̼������Һ�õ�����ZnCO3•2Zn��OH��2•H2O���������յõ�ZnO��
��1�����ݱ�������¶ȵȶԷ�Ӧ���ʵ�Ӱ���֪��Ϊ�������п��Ʒ���ܽ����ʣ��ɲ�ȡ�Ĵ�ʩ�н�����п��Ʒ�����ϸ����������������ᡢ���ȵȣ�����AΪ���ˣ��������õIJ��������У��ձ�����������©������ȱ��©����
�ʴ�Ϊ��������п��Ʒ�����ϸ����������������ᡢ���ȵȣ�©����
��2������������ۺ�����ͭ���ӡ������ӡ������Ӷ��ܷ�����Ӧ�����������ӡ�������ͭ���ʵȣ�������Ӧ�����ӷ���ʽ��2H++Fe=Fe2++H2����Cu2++Fe=Fe2++Cu��2Fe3++Fe=3Fe2+��
�ʴ�Ϊ��2H++Fe=Fe2++H2����Cu2++Fe=Fe2++Cu��2Fe3++Fe=3Fe2+��
��3������P��Fe��OH��2��Fe��OH��3�����ʵ���֮��Ϊ5��1���������ڿ��������տɻ�ø����ܵĴŷ�Fe3O4�����������غ㣬��Ӧ�����л�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��20Fe��OH��2+4Fe��OH��3+3O2=$\frac{\underline{\;����\;}}{\;}$8Fe3O4+26H2O��
�ʴ�Ϊ��20Fe��OH��2+4Fe��OH��3+3O2=$\frac{\underline{\;����\;}}{\;}$8Fe3O4+26H2O��
��4����450��500��������ZnCO3•2Zn��OH��2•H2O���ZnO���������ɶ�����̼�����ˮ����Ӧ�Ļ�ѧ����ʽΪ��ZnCO3•2Zn��OH��2•H2O$\frac{\underline{\;450��-500��\;}}{\;}$3ZnO+CO2��+3H2O����
�ʴ�Ϊ��ZnCO3•2Zn��OH��2•H2O$\frac{\underline{\;450��-500��\;}}{\;}$3ZnO+CO2��+3H2O����
��5��ȡ20.00mL��ҺN����O.02mol��L-l��KMnO4��Һ���еζ�������KMnO4��Һ18.00mL��������ص����ʵ���Ϊ��0.02mol/L��0.018L=0.00036mol��
����������ӱ�������ӣ����ϼ۽���5�ۣ��������ӱ�������ӻ��ϼ۱仯Ϊ1������߷�Ӧ�Ĺ�ϵʽΪ��KMnO4��5Fe2+��
��Ӧ���ĵ��������ӵ����ʵ���Ϊ��0.00036mol��5=0.0018mol��
����ҺN��Fe2+��Ũ��Ϊ��c��Fe2+��=$\frac{0.0018mol}{0.02L}$=0.09mol/L��
�ʴ�Ϊ��0.09mol/L��
���� ���⿼���������Ʊ���������ơ����ʷ������ᴿ�������ۺ�Ӧ�ã���Ŀ�ѶȽϴ���ȷ�Ʊ�����Ϊ���ؼ���ע�����ճ������ʷ������ᴿ�IJ�������������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ѧʵ�顢��ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ���Ҵ� | |
| B�� | �Ҷ������е�197.3�棩�����ᣨ�е�117.9�棩 | |
| C�� | �Ȼ�����Һ��̼��� | |
| D�� | ������Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.4g����þȫ�����þ����ʱʧȥ�ĵ�����Ϊ0.1NA | |
| B�� | 1.0 mol�κε�������ķ�������ΪNA��ԭ������Ϊ2NA | |
| C�� | 17gNH3�����ĵ�����ĿΪNA | |
| D�� | 16g 02��03��������У�����ԭ����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Fe��OH��3 | Fe��OH��2 | Al��OH��3 |
| ��ʼ����pH | 1.9 | 7.0 | 3.4 |
| ��ȫ����pH | 3.2 | 9.0 | 4.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��п������������иߴŵ��ʡ��ͽ������͵�����ĵ����ܣ��ѹ㷺Ӧ���ڵ��ӹ�ҵ��̼������Ҫ�����Ʊ���п���������壬����̼���̵�ԭ��֮һ�Ƕ������̣�ij��ѧ�о���ѧϰС����ӷϾɸɵ���л��ն���������ȡ̼���̣�
��п������������иߴŵ��ʡ��ͽ������͵�����ĵ����ܣ��ѹ㷺Ӧ���ڵ��ӹ�ҵ��̼������Ҫ�����Ʊ���п���������壬����̼���̵�ԭ��֮һ�Ƕ������̣�ij��ѧ�о���ѧϰС����ӷϾɸɵ���л��ն���������ȡ̼���̣�| ʵ�鲽�裨��Ҫ��д�����岽�裩 | Ԥ�ڵ�ʵ������ͽ��� |
| �����ó������ˡ�ϴ�ӣ� ��������ֱ�¶�ڿ����У��۲���ɫ | ��ɫ��ɺ�ɫ��˵������Mn��OH��2 |
| ȡ�����������Թ��У��������������ᣬ�۲����� | û���������ɣ�˵������MnCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a��A-N+m��}{A+m}$mol | B�� | $\frac{a��A-N��}{A+m}$ mol | C�� | $\frac{a��A-N+m��}{A+2m}$mol | D�� | $\frac{a��A-N+m��/}{A}$mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | X+3Y?2Z ����ӦΪ���ȷ�Ӧ | B�� | X+3Y?2Z ����ӦΪ���ȷ�Ӧ | ||
| C�� | X+2Y?3Z ����ӦΪ���ȷ�Ӧ | D�� | 5Z+3Y?4Z ����ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

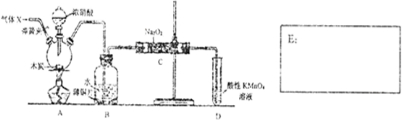
| A�� | ʵ��I����εμ�����ʱ���Թ������������������� | |
| B�� | ʵ��ɱȽ��ȡ�̼��������Ԫ�صķǽ�����ǿ�� | |
| C�� | ʵ��ӱ���ʳ��ˮ����ȡNaCl���� | |
| D�� | װ�â�������KMnO4��Һ�������ݳ��֣�����Һ��ɫ����dz������ȥ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com