
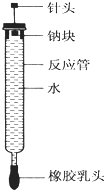
 有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.
有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.| a mL |
| V mL/mol |
| a |
| V |
| a |
| V |
| a |
| V |
| 2a |
| V |
| 2a |
| V |
| 46a |
| V |
| 46a |
| V |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、K+、MnO4-、SO42-、Cl- |
| B、Na+、K+、SO42-、Cl- |
| C、Na+、K+、I-、NO3- |
| D、Ca2+、HCO3-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由甲苯氧化制苯甲酸;苯与浓硝酸、浓硫酸混合共热制取硝基苯 |
| B、丙烯与溴水反应;乙炔一定条件下与氯化氢反应生成氯乙烯 |
| C、乙炔一定条件下反应生成苯;溴乙烷和NaOH醇溶液共热 |
| D、乙醇与浓硫酸共热至170℃生成乙烯; 乙醇与浓硫酸共热至140℃生成乙醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)已知下列两个热化学方程式:
(1)已知下列两个热化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
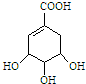 (1)按系统命名法命名.有机物CH3CH(C2H5)CH(CH3)2的名称是
(1)按系统命名法命名.有机物CH3CH(C2H5)CH(CH3)2的名称是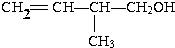
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第1列元素均能形成M2O和M2O2型化合物 |
| B、第14列元素所形成的化合物种类最多 |
| C、第17列元素均有最高价氧化物R2O7 |
| D、最外层有两个电子的原子都在第2列 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com