
【题目】当光束通过下列分散系:①尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔现象的是( )
A.①②
B.②③
C.①④
D.②④
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】聚乙二醇(PEG) 是一种用途广泛的聚合物,1,2-乙二醇碳酸酯(又称为碳酸亚乙酯) 是一种医药中间体。某小组以烃A 为原料合成PEG和碳酸亚乙酯的路线设计如下: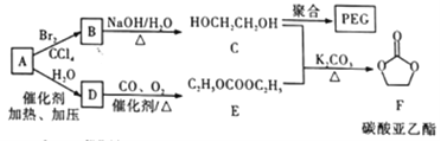
已知: 2C2H5OH+CO+1/2O2 ![]() C2H5OCOOC2H5+H2O
C2H5OCOOC2H5+H2O
回答下列问题:
(1)A的名称为____________; A→B的反应类型为__________;C 的核磁共振氢谱中峰面积比为___________;F的分子式为____________________。
(2)B→C的化学方程式为____________。
(3)C在一定条件下发生聚合反应生成PEC,化学方程式为___________________;若某种PEG的平均相对分子质量为2000, 则其平均聚合度为____________________。
(4)E的同分异构体中,含有—OCOO—基团的共有___种(不包含E和立体异构)。
(5)有人认为C和E生成F的反应历程可能如下:
①HOCH2CH2OH + CO32-![]() HOCH2CH2O-+HCO3-
HOCH2CH2O-+HCO3-
②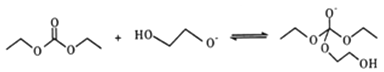
③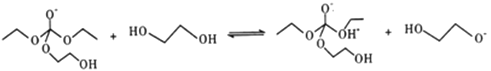
④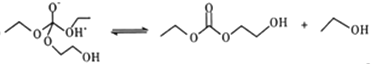
⑤
⑥⑦⑧……
⑨HOCH2CH2O- +HCO3-→HOCH2CH2OH+CO32-
写出上述历程中⑥⑦⑧的反应方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是 ( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是 ( )
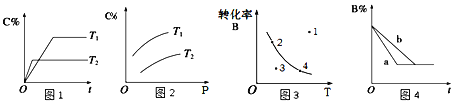
A. 由图1可知,T1<T2,该反应正反应为吸热反应
B. 由图2可知,该反应m+n﹤p
C. 图3中,表示反应速率v正>v逆的是点3
D. 图4中,若m+n=p,则a曲线一定使用了催化剂
【答案】C
【解析】A. 由图1可知,T2时达到平衡所需时间短,所以T1<T2,升温平衡左移,该反应正反应为放热反应,故A错误;B. 由图2可知,加压平衡右移,说明该反应m+n>p,故B错误;C. 图3中,温度一定,点3达到平衡的过程中B减少,V正>V逆,故C正确;D. 图4中,若m+n=p,加压平衡不移动,则a曲线可能为加压,故D错误。故选C。
点睛:在分析本题图1和图4一类涉及影响反应速率条件的图像时,注意把握图像的关键内容—斜线的斜率,斜率越大,反应速率越大,对应的是有利于增大反应速率的条件。
【题型】单选题
【结束】
11
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行反应:X(g)+2Y(g)![]() 3Z(g)+Q(s) △H >0,下列叙述正确的是
3Z(g)+Q(s) △H >0,下列叙述正确的是
A. 当容器中X与Y的物质的量的比满足1:2时反应达到平衡
B. 达到平衡时X的转化率为25%,则平衡常数K值为9/4
C. 达到平衡后,反应速率2V正(Y)="3" V逆(Z)
D. 达到平衡后,加入Q,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是
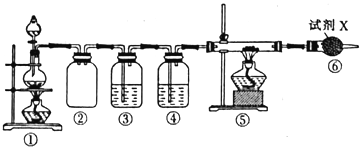
A. ①中发生的化学反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B. ④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰
C. ③中盛放的试剂是NaOH 溶液
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子, X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:
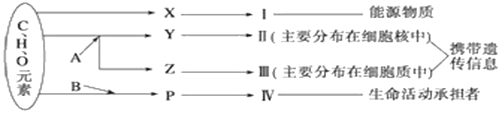
(1)Ⅰ在小麦种子中主要是指______,其基本单位X是______。
(2)A代表的元素是____,Ⅱ是____,Ⅲ是RNA,Z是_____。
(3)Ⅳ一定含有的元素有______。P的结构通式是______,图中由P形成Ⅳ的反应方式称为____,Ⅳ的特定功能的发挥与其_____结构有关。若P的平均相对分子质量r,由多个P形成m条肽链,经盘曲折叠形成了相对分子质量为e的Ⅳ,则Ⅳ分子中肽键的数目是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火力发电厂释放出大量氮的氧化物(NOx)、二氧化硫等气体会造成环境污染,对燃煤废气进行脱除处理。可实现绿色环保、低碳减排、废物利用等目的。
(1)己知:N2 (g) +O2 (g) =2NO (g) △H=+180.5kJ·mol-1
C (s) +O2 (g)=CO2 (g) △H=-393.5 kJ·mol-1
2C (s) +O2(g) =2CO (g)△H=-221 kJ·mol-1
若某反应的平衡常数表达式为: 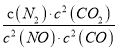 ,请写出此反应的热化学方程式_________。
,请写出此反应的热化学方程式_________。
(2)脱硝
利用甲烷与NO2反应,生成无污染的物质,则该反应的化学方程式为:___________。
(3)脱碳
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线(见如图1),则上述CO2转化为甲醇反应的△H3_____0(填“>”、“<”或“=”)。
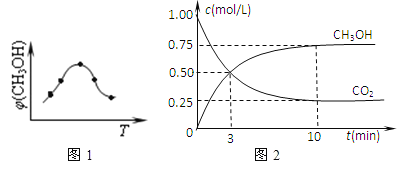
②在一恒温恒容密闭容器中充入0.5molCO2和1.5molH2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如上图2所示.请回答:第10min后,若升温,该反应的平衡常数将_____(填“变大”、“变小”、“不变”);若向该容器中再充入1molCO2和3molH2再次达到平衡时,则CH3OH(g)的体积分数将___(“变大”、“变小”、“不变”)。
(4)脱硫
某种脱硫工艺中将废气经处理后,与一定量的氨气、潮湿的空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.设烟气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为__________。若在0.1mol/L的硝酸铵溶液中加入等体积的0.09mol/L氨水,配制了pH=8.2的溶液,则该溶液中微粒浓度由大到小的顺序为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,充入一定量的反应物A,反应![]() 达平衡后,保持温度不变,将容器体积缩到一半,当达到新的平衡时,B的浓度是原来的1.6倍,则
达平衡后,保持温度不变,将容器体积缩到一半,当达到新的平衡时,B的浓度是原来的1.6倍,则
A. 平衡向正反应方向移动了 B. 物质A的转化率降低
C. 物质B的质量增加 D. ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com