

| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为 | |
| C. | 与w同主族的某元素形成的18电子的氢化物分子中只有共价键没有离子键 | |
| D. | Q可形成多种含氧酸 |
分析 这几种元素是短周期元素,根据元素在周期表中的位置知,Q、R是第二周期元素,T、W是第三周期元素,四种元素只有一种元素,则只能是T为金属元素,为Al元素,所以Q是C、R是N、W是S元素.
A.元素非金属性越强,其气态氢化物稳定性越强;
B.铝离子质子数为13,核外电子层为10,有2个电子层,各层电子数为2、8;
C.与w同主族的某元素形成的18电子的氢化物分子为H2O2;
D.Q为碳元素,可以形成碳酸、有机酸等.
解答 解:这几种元素是短周期元素,根据元素在周期表中的位置知,Q、R是第二周期元素,T、W是第三周期元素,四种元素只有一种元素,则只能是T为金属元素,为Al元素,所以Q是C、R是N、W是S元素.
A.非金属R>Q,所以气态氢化物的稳定性R>Q,故A正确;
B.铝离子质子数为13,核外电子层为10,有2个电子层,各层电子数为2、8,原子结构示意图为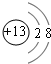 ,故B错误;
,故B错误;
C.与w同主族的某元素形成的18电子的氢化物分子为H2O2,只含有共价键,不含离子键,故C正确;
D.Q为碳元素,可以形成碳酸、有机酸等,可以形成多种含氧酸,故Q正确,
故选B.
点评 本题侧重考查元素周期表结构、元素周期律,D选项为易错点,学生容易忽略有机酸,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 26Fe的价层电子排布式为3d64s2 | |
| B. | 35Br的电子排布式可简写为[Ar]4s24p5 | |
| C. | NH4Cl的电子式为  | |
| D. | 氯离子结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | ||
| M |
 N2+2CO2,该反应的平衡常数表达式为K=$\frac{c(C{O}_{2})•c({N}_{2})}{{c}^{2}(CO)•{c}^{2}(NO)}$;
N2+2CO2,该反应的平衡常数表达式为K=$\frac{c(C{O}_{2})•c({N}_{2})}{{c}^{2}(CO)•{c}^{2}(NO)}$;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:r(Y2-)>r(Z2+) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | Y的气态简单氢化物的热稳定性比氮元素的气态简单氢化物弱 | |
| D. | X、Y、Z、W所有元素的最高正价等于其所在族的族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
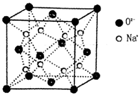 (1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等.
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
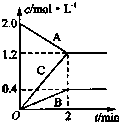 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=0的某溶液 | B. | 0.1 mol•L-1 NaOH 溶液 | ||
| C. | 0.1mol•L-1 HCl 溶液 | D. | 0.1 mol•L-1的 NaCl 溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
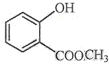 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.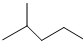 表示的分子式为C6H14;2-甲基-2-丁烯的结构简式为CH3C (CH3)=CHCH3.
表示的分子式为C6H14;2-甲基-2-丁烯的结构简式为CH3C (CH3)=CHCH3.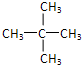 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原原理 | B. | 溶解沉淀原理 | C. | 平衡移动原理 | D. | 物质两性原理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com