
| ĪĀ¶Č”ę | 450 | 500 | 550 | 600 |
| SO2µÄ×Ŗ»ÆĀŹ% | 97.5 | 95.8 | 90.50 | 80.0 |
·ÖĪö £Ø1£©ÉżøßĪĀ¶Č£¬æÉÄę·“Ó¦ĻņĪüČČ·“Ó¦·½ĻņŅĘ¶Æ£¬øł¾ŻĘ½ŗā³£ŹżÓėĪĀ¶Č±ä»Æ¹ŲĻµČ·¶ØģŹ±ä£»
£Ø2£©µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷ĪļÖŹµÄÅØ¶Č”¢°Ł·Öŗ¬Įæ²»±ä£¬ŅŌ¼°ÓÉ“ĖŃÜÉśµÄŅ»Š©ĮæŅ²²»·¢Éś±ä»Æ£¬¾Ż“Ė½ā“š£¬½āĢāŹ±ŅŖ×¢Ņā£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£»
£Ø3£©¼ĘĖćĘ½ŗāŹ±ø÷×é·ÖµÄĘ½ŗāÅØ¶Č£¬“śČėĘ½ŗā³£Źż±ķ“ļŹ½¼ĘĖć£»
£Ø4£©Ń¹ĒæŌö“ó£¬Ę½ŗāĻņĘųĢåĢå»ż¼õÉŁµÄ·½ĻņŅĘ¶Æ£®
½ā“š ½ā£ŗ£Ø1£©ÉżøßĪĀ¶Č£¬Ę½ŗāĻņĪüČČ·½ĻņŅĘ¶Æ£¬øł¾Ż±ķøńÖŖ£¬ĪĀ¶ČŌ½øߣ¬»ÆŃ§Ę½ŗā³£ŹżŌ½Š”£¬ĖµĆ÷Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬¼“”÷H£¼0£¬
¹Ź“š°øĪŖ£ŗ£¼£»
£Ø2£©A£®Ėę·“Ó¦½ųŠŠĘųĢåµÄĪļÖŹµÄĮæ¼õÉŁ£¬Ń¹Ēæ¼õÉŁ£¬ČŻĘ÷ÖŠŃ¹Ēæ²»±ä£¬ĖµĆ÷µ½“ļĘ½ŗāדĢ¬£¬¹ŹAÕżČ·£»
B£®Ėę·“Ó¦½ųŠŠĘųĢåµÄÖŹĮæ²»±ä£¬ČŻĘ÷µÄĢå»żŅ²²»±ä£¬ĆÜ¶Č²»±ä£¬»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä£¬²»ÄÜĖµĆ÷µ½“ļĘ½ŗāדĢ¬£¬¹ŹB“ķĪó£»
C£®»ģŗĻĘųĢåÖŠSO3µÄÅØ¶Č²»±ä£¬ÄÜĖµĆ÷µ½“ļĘ½ŗāדĢ¬£¬¹ŹCÕżČ·£»
D£®·“Ó¦µ½“ļĘ½ŗāŹ±øöĪļÖŹµÄÅØ¶Č²»±ä£¬µ«²»Ņ»¶ØC£ØSO2£©=C£ØSO3£©£¬ĖłŅŌ²»ÄÜ×÷ĪŖ“ļĘ½ŗāדĢ¬µÄ±źÖ¾£¬¹ŹD“ķĪó£»
E£®ŌŚČĪŗĪŹ±æĢvÕż£ØSO2£©=vÕż£ØSO3£©£¬ĖłŅŌ²»ÄÜ×÷ĪŖ“ļĘ½ŗāדĢ¬µÄ±źÖ¾£¬¹ŹE“ķĪó£»
F£®vÕż£ØSO3£©=2vÄę£ØO2£©²»Ķ¬ĪļÖŹ±ķŹ¾µÄĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬ĖµĆ÷µ½“ļĘ½ŗāדĢ¬£¬¹ŹFÕżČ·£»
¹ŹŃ”£ŗACF£»
£Ø3£©2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£¬
·“Ó¦æŖŹ¼£Ømol/L£© 0.4 1 0
·“Ó¦£Ømol/L£© 0.32 0.16 0.32
Ę½ŗā £Ømol/L£© 0.08 0.84 0.32
Ę½ŗā³£ŹżK=$\frac{0.3{2}^{2}}{0.0{8}^{2}”Į0.84}$=$\frac{400}{21}$£¬
¹Ź“š°øĪŖ£ŗ$\frac{400}{21}$£»
£Ø4£©øĆ·“Ó¦ÕżĻņŹĒŅ»øöĘųĢåĢå»ż¼õÉŁµÄ·“Ó¦£¬ĖłŅŌŃ¹ĒæŌö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¹Ź“š°øĪŖ£ŗÕż£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓ°Ļģ»ÆŃ§Ę½ŗāŅĘ¶ÆµÄŅņĖŲ”¢Ę½ŗāדĢ¬µÄÅŠ¶Ļ”¢·“Ó¦ĖŁĀŹµÄ¼ĘĖć”¢Ę½ŗā³£ŹżµÄ¼ĘĖćµČÖŖŹ¶µć£¬×¢ŅāĄūÓĆČż¶ĪŹ½¼ĘĖćĘ½ŗāŹ±ø÷×é·ÖµÄĘ½ŗāÅØ¶Č£¬“śČėĘ½ŗā³£Źż±ķ“ļŹ½¼ĘĖć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
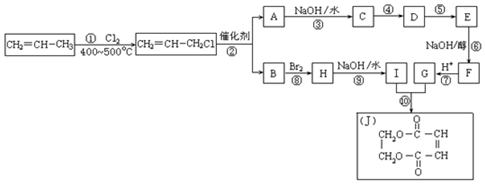
 Į½±ß»łĶÅ»»Ī»µÄ·“Ó¦£®ČēĮ½øö±ūĻ©·Ö×Ó½ųŠŠĻ©Ģž»»Ī»£¬Éś³É¶”Ļ©ŗĶŅŅĻ©£®
Į½±ß»łĶÅ»»Ī»µÄ·“Ó¦£®ČēĮ½øö±ūĻ©·Ö×Ó½ųŠŠĻ©Ģž»»Ī»£¬Éś³É¶”Ļ©ŗĶŅŅĻ©£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ°²»ÕŹ”»ĘɽŹŠøßČżÉĻŌĀ漶ž»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
X”¢Y”¢Z”¢W”¢RŹĒ5ÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£XŹĒÖÜĘŚ±ķÖŠŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬YŌ×Ó×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ3±¶£¬Z”¢W”¢R“¦ÓŚĶ¬Ņ»ÖÜĘŚ£¬RÓėY“¦ÓŚĶ¬Ņ»×壬Z”¢WŌ×ÓµÄŗĖĶāµē×ÓŹżÖ®ŗĶÓėY”¢RŌ×ÓµÄŗĖĶāµē×ÓŹżÖ®ŗĶĻąµČ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ĪļÖŹAÓÉZÓėYĮ½ÖÖŌŖĖŲ×é³É£¬Ōņ0.5 molĪļÖŹAÖŠŗ¬ÓŠµÄĄė×ÓŹżŌ¼ĪŖ9.03”Į1023
B. ŌŖĖŲY”¢Z”¢WŠĪ³ÉµÄĄė×Ó¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹£¬ĘäĄė×Ó°ė¾¶ŅĄ“ĪŌö“ó
C. ŌŖĖŲZ”¢RµÄŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼äĻą»„·“Ӧɜ³ÉµÄŃĪČÜŅŗ³ŹÖŠŠŌ»ņ¼īŠŌ
D. ŌŖĖŲY”¢R·Ö±šÓėŌŖĖŲXŠĪ³ÉµÄ»ÆŗĻĪļµÄ·Šµć£ŗXmY £¼ XmR
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģÖŲĒģŅ»ÖŠøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
²ÄĮĻ”¢ÄÜŌ“”¢ŠÅĻ¢”¢»·¾³Óė»Æѧ¹ŲĻµĆÜĒŠ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®ĪŅĆĒŹ¹ÓĆŗĻ½šŹĒŅņĪŖĖü±Č“潚Źō¾ßÓŠøüÓÅĮ¼µÄ»śŠµŠŌÄÜ
B£®øֻƲ£Į§”¢ÓŠ»ś²£Į§”¢ŹÆÓ¢²£Į§¾łŹōÓŚ¹čĖįŃĪ²ÄĮĻ
C£®øßĢśĖį¼Ų£ØK2FeO4£©ŹĒŅ»ÖÖŠĀŠĶ”¢øߊ§”¢¶ą¹¦ÄÜĖ®“¦Ąķ¼Į£¬¼ČÄÜɱ¾śĻū¶¾ÓÖÄܾ»Ė®
D£®øß“æ¶ČµÄ¶žŃõ»Æ¹č¹ć·ŗÓĆÓŚÖĘ×÷¹āµ¼ĻĖĪ¬£¬¹āµ¼ĻĖĪ¬ÓöĒæ¼ī»į”°¶ĻĀ·”±
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¶ž¼×ĆŃ£ØCH3OCH3£©ŹĒŅ»ÖÖÓ¦ÓĆĒ°¾°¹ćĄ«µÄĒå½ąČ¼ĮĻ£¬ŅŌCOŗĶH2ĪŖŌĮĻÉś²ś¶ž¼×ĆŃÖ÷ŅŖ·¢ÉśŅŌĻĀČżøö·“Ó¦£ŗ
¶ž¼×ĆŃ£ØCH3OCH3£©ŹĒŅ»ÖÖÓ¦ÓĆĒ°¾°¹ćĄ«µÄĒå½ąČ¼ĮĻ£¬ŅŌCOŗĶH2ĪŖŌĮĻÉś²ś¶ž¼×ĆŃÖ÷ŅŖ·¢ÉśŅŌĻĀČżøö·“Ó¦£ŗ| ±ąŗÅ | ČČ»Æѧ·½³ĢŹ½ | »ÆŃ§Ę½ŗā³£Źż |
| ¢Ł | CO£Øg£©+2H2£Øg£©?CH3OH£Øg£©”÷H1 | K1 |
| ¢Ś | 2CH3OH£Øg£©?CH3OCH3£Øg£©+H2O£Øg£©”÷H2=-24kJ•mol-1 | K2 |
| ¢Ū | CO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H3=-41kJ•mol-1 | K3 |
| »Æѧ¼ü | H-H | C-O | C=O | H-O | C-H |
| E/£ØkJ£®mol-1£© | 436 | 343 | 1076 | 465 | 413 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com