
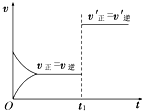
 对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:| A. | ②③ | B. | ①② | C. | ③④ | D. | ④⑤ |
分析 由图象可知,t1时刻改变条件,正逆反应速率均增大相同的倍数,平衡不移动,可以使用催化剂,对于反应前后气体体积不变的可逆反应,也可以增大压强,结合外界条件对反应速率、平衡移动影响分析解答.
解答 解:由图象可知,t1时刻改变条件,正逆反应速率均增大相同的倍数,平衡不移动,
①加入A,改变条件瞬间,正反应速率增大、逆反应速率不变,平衡向正反应方向移动,故①不符合;
②加入催化剂,同等程度增大正、逆反应速率,平衡不移动,故②符合;
③该反应前后气体的体积不变,加压,同等程度增大正、逆反应速率,平衡不移动,故③符合;
④正反应为吸热反应,升温,正反应速率增大倍数大于逆反应速率增大倍数,平衡向正反应方向移动,故④不符合;
⑤若全部移走C,不影响气体组分的浓度,瞬间正、逆反应速率不变,但由于生成物C全部被移走,反应不能向逆反应进行,导致平衡向正反应方向移动,若部分移走C,正、逆反应速率不变,故⑤不符合,
故选:A.
点评 本题考查外界条件对反应速率、平衡移动的影响,难度中等,注意⑤分析为易错点,学生容易若为C为固体,移走C平衡不移动,忽略全部移走C的情况.


科目:高中化学 来源: 题型:选择题
| A. | 液氯不导电是非电解质,氯水能导电是强电解质 | |
| B. | 在常温常压下,11.2升氯气所含的原子数目为NA | |
| C. | 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 | |
| D. | 1mol氯气参加反应,转移的电子数一定为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
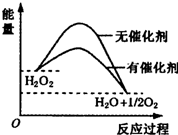
| A. | H2O2分解反应的△H>0 | |
| B. | 催化剂的加入使反应的热效应减小 | |
| C. | 催化剂的加入提高了H2O2的分解率 | |
| D. | 催化剂通过改变反应历程、降低反应的活化能来提高H2O2分解速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱、烧碱均属于碱 | |
| B. | CuSO4•5H2O、液氨均属于纯净物 | |
| C. | 凡能电离出H+的化合物均属于酸 | |
| D. | NaCl H2SO4 BaSO4 NH3均属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨是弱电解质,铵盐是强电解质 | |
| B. | 液氨是纯净物,氨水是混合物 | |
| C. | 氨气遇浓盐酸、浓硫酸、浓硝酸都能产生白烟 | |
| D. | 氨气易液化,所以可用来做喷泉实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com