
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
分析 (1)依据平衡常数随温度的变化结合平衡移动原理分析判断反应的热量变化,根据表中数据可知,温度升高平衡常数减小,说明平衡向逆反应方向移动;根据反应方程式及化学平衡常数表达式完成;
(2)根据达到化学平衡状态,各组分浓度不变,正逆反应相等进行分析;
(3)根据实际生产中,即要考虑反应速率又要考虑转化率,还要兼顾设备并结合反应特征分析;
(4)依据平衡三段式列式计算反应的一氧化碳,根据转化率概念计算得到;
(5)为使该反应的反应速率增大,可采用增大压强、升高温度、加入催化剂、增大反应物浓度等方法,再结合平衡移动原理分析解答.
解答 解:(1)根据表中数据可知,温度升高平衡常数减小,说明平衡向逆反应方向移动,则正反应放热,根据反应CO(g)+H2O(g)?H2(g)+CO2(g)及化学平衡常数表达式,K=$\frac{c({H}_{2})•c(C{O}_{2})}{c(CO)•c({H}_{2}O)}$,
故答案为:放热;K=$\frac{c({H}_{2})•c(C{O}_{2})}{c(CO)•c({H}_{2}O)}$;
(2)a.反应前后气体体积不变,压强始终不会变化,所以压强不变,无法判断是否达到平衡状态,故a错误;
b.浓度不变,反应达到了化学平衡状态,故b正确;
c.正逆反应速率相等,各组分浓度不变,达到了化学平衡状态,故c正确;
d.浓度相等,不能判断各组分浓度是否不变,无法判断是否达到平衡状态,故d错误;
故答案为:bc;
(3)实际生产中,即要考虑反应速率又要考虑转化率,还要兼顾设备,所以由于反应前后气体体积不变,又是放热反应,故温度不宜太高,所以常压,400~500℃催化剂最好,
故答案为:C;
(4)830℃时,在2L的密闭容器中加入4molCO(g)和6molH2O(g)达到平衡时,设一氧化碳转化物质的量为x,
CO(g)+H2O(g)?H2(g)+CO2(g)
起始量(mol) 4 6 0 0
变化量(mol) x x x x
平衡量(mol) 4-x 6-x x x
平衡常数K=$\frac{{x}^{2}}{(4-x)•(6-x)}$=1,解得:x=2.4mol,
所以CO2的平衡浓度为:$\frac{2.4mol}{2L}$=1.2mol/L
用H2浓度变化来表示的平均反应速率=$\frac{\frac{2.4mol}{2L}}{10min}$=0.12mol/(L•min)
CO的转化率=$\frac{2.4mol/L}{4mol}$×100%=60%,
故答案为:1.2mol/L;0.12mol/(L•min);60%;
(5)a.增大CO的浓度反应速率增大,且该反应向正反应方向移动,故正确;
b.升高温度,反应速率增大但平衡向逆反应方向移动,故错误;
c.分离生成物平衡向右移动,但反应速率减小,故错误;
d.选择高效催化剂能增大反应速率,但平衡不移动,故错误;
故答案为:a.
点评 本题考查了化学平衡的计算,题目难度中等,明确影响化学平衡的因素为解答关键,注意掌握三段式在化学平衡的计算中的应用,试题培养了学生的分析能力及化学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表中,Y所在族的元素都是活泼金属元素 | |
| B. | 37Z原子核电子数为20 | |
| C. | X与Y能形成YX型化合物 | |
| D. | 在常温下,Z的单质与氢气一定能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
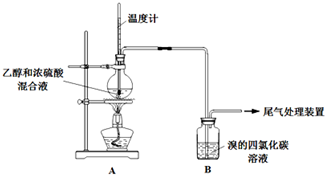
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |

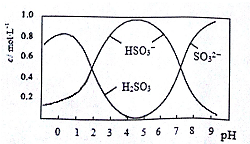
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 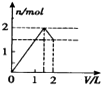 | C. | 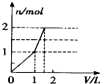 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,稀释0.1mol/L的CH3COOH溶液,KW不变,Ka将增大 | |
| B. | 对FeCl3溶液进行稀释时,Fe3+水解程度将增大,故溶液的酸性将增强 | |
| C. | 可根据Ksp的数值大小直接比较难溶物在水中的溶解度大小 | |
| D. | 25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl悬浊液中加入KI固体,有黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁跟硫酸铜溶液反应:2Fe+3Cu2+═2Fe3++3Cu | |
| B. | 碳酸钙跟醋酸反应CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| C. | 在碳酸氢钙溶液中加入盐酸CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com