
科目:高中化学 来源:2014-2015甘肃省天水市高二下学期第一次月考化学试卷(解析版) 题型:选择题
要对热稳定的高沸点液态有机物和低沸点的杂质的混合物进行提纯一般使用( )的方法
A.重结晶 B.蒸馏 C.过滤 D.萃取
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:推断题
(16分)香豆素是用途广泛的香料,合成香豆素的路线如下(其他试剂、产物及反应条件均省略):

(1)Ⅰ的分子式为 ;1molⅠ与足量氧气完全燃烧消耗氧气的物质的量为 mol。
(2)物质Ⅳ中含氧官能团的名称 ,反应④的反应类型是 。
(3)香豆素在过量NaOH溶液中完全反应的化学方程式为 。
(4)Ⅴ是香豆素的同分异构体,写出符合下列条件的Ⅴ的结构简式 。
①苯环上只有两个处于对位的取代基②能使氯化铁溶液呈紫色 ③能发生银镜反应
(5)一定条件下,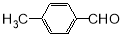 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省皖北协作区高三3月联考理综化学试卷(解析版) 题型:选择题
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是
A.Na+、Fe3+、NO3-、Cl2都可在该物质的溶液中大量共存
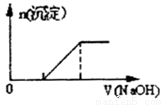
B.向0.1mo1/L该物质的溶液中清加0.L/molNaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如上图所示
C.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D.向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42--完全沉淀的离子方程式为:Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:选择题
室温下,将一定浓度的一元酸HA溶液和一定浓度的NaOH溶液等体积混合(忽略体积变化),实验数据如下表:

下列判断不正确的是
A.实验①反应的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
B.实验①反应的溶液中:c(OH-)= c(Na+)-c(A-)=Kw/(1×10-9)mol/L
C.实验②反应的溶液中:c(A-)+c(HA)>0.1mol/L
D.实验②反应的溶液中:c(Na+)= c(A-)> c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:填空题
(15分)2013年以来,我国多地频现种种极端天气。二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解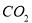 ,发生反应:
,发生反应: =2CO(g)+
=2CO(g)+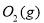 △H>0,该反应的
△H>0,该反应的 S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
(2)活性炭可用于处理大气污染物NO。在1 L恒容密闭容器中加入0.100 mol NO和2.030 mol固体活性炭(无杂质),生成气体E和气体F。当温度分别在 和
和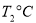 时,测得平衡时各物质的物质的量如下表:
时,测得平衡时各物质的物质的量如下表:
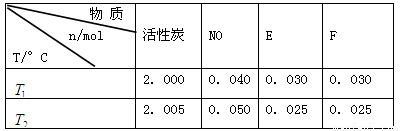
①请结合上表数据,写出NO与活性炭反应的化学方程式: 。
②上述反应在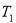 ℃时的平衡常数为
℃时的平衡常数为 ,在
,在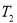 ℃时的平衡常数为
℃时的平衡常数为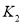 。
。
计算 = 。根据上述信息判断,
= 。根据上述信息判断, 和
和 的关系是 。
的关系是 。
a.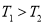 b.
b.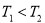 c.无法比较
c.无法比较
③在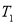 ℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(3)碘循环工艺不仅能吸收 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:
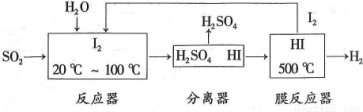
①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出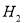 的目的是: 。
的目的是: 。
(4)开发新能源是解决大气污染的有效途径之一。直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:
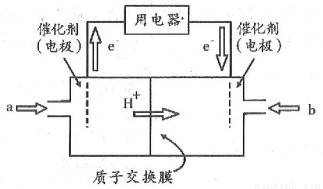
通过a气体的电极是原电池的 极(填“正”或“负”),其电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:选择题
已知第三周期元素M,其原子的最外层达到饱和时所需电子数小于次外层与最内层电子数之差,且等于最内层电子数的正整数倍,下列关于元素M的说法一定错误的是
A.M元素存在同素异形体
B.M元素为非金属元素
C.M的最高价氧比物对应的水化物都是强酸
D.常温下,能稳定存在的M的氧化物都是酸性氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:填空题
(12分)(选做题)本题包括A、B两小题,请选定其中一小题并作答。若多做,则按A小题评分。
A.[物质结构与性质]
尿素(H2NCONH2)是一种农业生产中常用的氮肥。在工业上,尿素还用于制造有机铁肥,如[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]。
(1)基态Fe3+的核外电子排布式为________。
(2)C、N、O三种元素的第一电离能由小到大的顺序是________。
(3)六氰合亚铁离子(Fe(CN) )中的配体CN-中C原子的杂化轨道类型是________,写出一种与CN-互为等电子体的单质分子的结构式________。
)中的配体CN-中C原子的杂化轨道类型是________,写出一种与CN-互为等电子体的单质分子的结构式________。
(4)在一定条件下,NH3与CO2能合成尿素,1 mol尿素分子中,σ键的数目为________。
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为________。

查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于SO2的说法中,不正确的是
A.SO2不能用来漂白食品
B.SO2与水反应生成H2SO4
C.SO2具有漂白性,可以使品红溶液褪色
D.SO2是一种大气污染物,它主要来自于化石燃料的燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com