

分析 (1)高铁酸根离子具有强氧化性,所以能杀菌消毒,高铁酸根离子能发生氧化还原反应生成氧气,同时生成氢氧化铁,氢氧化铁具有吸附性;
(2)根据图象中各粒子的存在情况与溶液pH的关系对各选项进行判断;
(3)由图2数据可知,将试样分别置于不同温度的恒温水浴中,来测定c(FeO42-)的变化,显然是确定温度对FeO42-浓度的影响情况.
解答 解:(1)高铁酸根离子具有强氧化性,所以能杀菌消毒,高铁酸根离子和水反应生成氢氧化铁胶体,胶体具有吸附性,所以能净水,反应的离子方程式为:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑,
故答案为:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑;
(2)A.不同PH值时,溶液中铁元素的存在形态及种数不相同,比如在PH值等于6时,就只有两种形态,故A错误;
B.根据图片知,向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数先增大,后减小,故B错误;
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O,故C正确;
故答案为:AB;
(3)由图2数据可知,温度越高,相同时间内FeO42-浓度变化越快,且高铁酸钾溶液平衡时FeO42-浓度越小,所以该操作的目的是探究温度变化对FeO42-浓度的影响,
故答案为:探究温度变化对c(FeO42-)的影响.
点评 本题考查了盐的水解原理及其应用,题目难度中等,涉及胶体的净水原理、离子方程式书写、盐的水解原理及其影响等知识,试题知识点较多,充分考查了学生灵活应用基础知识的能力.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
 咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )
咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )| A. | 该物质中苯环上一氯化物有2种 | |
| B. | 所有碳原子不可能都在同一平面上 | |
| C. | 既能发生取代反应,也能发生加成反应 | |
| D. | 1mol该物质可以与1.5mol碳酸钠溶液反应生成1.5molCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=1的溶液中还可以大量存在:K+、MnO4-、SO42-、CH3CHO | |
| B. | 含有较多Fe3+的溶液中还可以大量存在:Na+、SO42-、SCN-、CO32- | |
| C. | 碳酸氢钙溶液与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 向FeBr2溶液中通入过量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
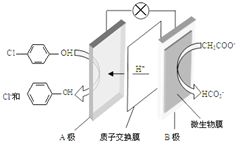 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(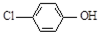 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )| A. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA | |
| B. | A极的电极反应式为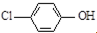 +e-═Cl-+ +e-═Cl-+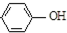 | |
| C. | 电流方向从B极沿导线经小灯泡流向A极 | |
| D. | B为电池的正极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1mol甲基(14C1H3-)所含的中子数和电子数分别为8NA、10NA | |
| B. | 标准状况下,11.2L五氯化磷中含有P-Cl键的数目为2.5NA | |
| C. | 标准状况下,2.24L Cl2全部被NaOH溶液吸收,转移的电子数目为0.2NA | |
| D. | 已知反应:2NH3+NO+NO2═2N2+3H2O,每生成2molN2转移的电子数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用如图装置可以制取某些气体,所用药品合理且收集气体方法正确的是( )
利用如图装置可以制取某些气体,所用药品合理且收集气体方法正确的是( )| 制取气体 | 实验药品 | 收集气体方法 | |
| A | 二氧化碳 | 碳酸钙、稀硫酸 | 排饱和碳酸氢钠溶液 |
| B | 氧气 | 双氧水、二氧化锰 | 排水法 |
| C | 氨气 | 氧氡化钠溶液、浓氨水 | 向下排空气法 |
| D | 乙烯 | 氯乙烷,氢氧化钠、乙醇 | 排水法 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在沸腾炉和接触室中,均使用过量的高压空气,以提高硫铁矿的燃烧利用率和二氧化硫的催化氧化转化率 | |
| B. | 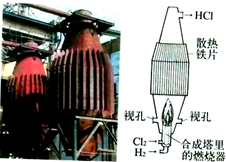 如图是工业制盐酸的设备及其简易图 | |
| C. | 氯碱工业是中国现代化工之母,其主要反应是电解海水,得到烧碱和氯气,因此称为氯碱工业 | |
| D. | 合成氨工业是工业制硝酸和工业制纯碱的前提和保证,前者可为后两者共提供了不止一种原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
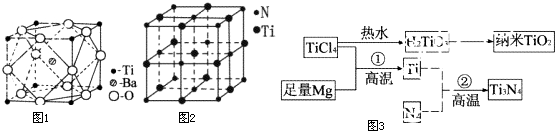
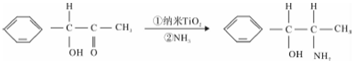
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com