
【题目】短周期元素W、X、Y、Z的原子序数依次增加,由这些元素组成的常见物质的转化关系如下图,其中a、b、d、g为化合物,a为淡黄色固体,c是Z的单质,在铝热反应中常做引发剂;e、f为常见气体单质。下列有关说法正确的是( )

A. 简单离子的半径:Y>Z>X
B. 简单氢化物的沸点:Y>X
C. 最高价氧化物对应水化物的碱性:Z> Y
D. Y、Z的氧化物所含化学键类型相同
【答案】B
【解析】
短周期元素W、X、Y、Z的原子序数依次增加,其中a、b、d、g为化合物,a为淡黄色固体,则a为过氧化钠;c是Z的单质,在铝热反应中常做引发剂,c为金属镁;e、f为常见气体单质,根据框图,镁与化合物b反应生成气体单质f,则f为氢气;过氧化钠与化合物b反应生成气体单质e,则e为氧气,则b为水,d为氢氧化钠,g为氢氧化镁。
根据上述分析,a为过氧化钠, b为水,c为镁,d为氢氧化钠,e为氧气,f为氢气,g为氢氧化镁;则W为H、X为O、Y为Na、Z为Mg;
A. X为O、Y为Na、Z为Mg,简单离子具有相同的电子层结构,离子半径: X>Y>Z,故A错误;
B.X为O,Y为Na,氢化钠是离子化合物,沸点高于水,故B正确;
C. 金属性越强,最高价氧化物对应水化物的碱性越强,Z为镁,Y为钠,所以碱性:Y>Z ,故C错误;
D. Y的氧化物有氧化钠和过氧化钠,氧化钠中只含有离子键,而过氧化钠中既有离子键又有共价键,Z的氧化物为MgO,MgO中只含离子键,所以所含化学键类型不相同,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法中不正确的是( )
元素编号 | |||||||
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
原子半径 | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
最高正化合价 | 无 |
|
|
|
|
|
|
最低负化合价 |
|
| 无 |
|
| 无 | 无 |
A.⑦的简单离子不是同周期元素离子半径最小的
B.①元素的氢化物有两种
C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏
D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如图:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)![]() 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为____;砷酸的第一步电离方程式为______。
(2)“一级沉砷”中FeSO4的作用是_____;“二级沉砷”中H2O2与含砷物质反应的化学方程式为_______。
(3)沉淀X为____(填化学式)。
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
(4)AsH3的电子式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有100mLMgCl2和AlCl3的混合溶液,其中 c(Mg2+)=0.30mol·L-1,c(Cl-)=1.20 mol·L-1,要使Mg2+完全转化为Mg(OH)2且与Al3+恰好分开,至少需要1.00 mol·L-1的NaOH溶液的体积为
A. 80 mLB. 100 mLC. 120 mLD. 140 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.用相应的方程式解释:
(1)NaHSO3溶液显酸性:___________________
(2)NaHCO3溶液显碱性:____________________
(3)NH4Cl溶液显酸性:______________________
(4)明矾[KAl(SO4)2]净水:___________________
(5)FeCl3溶液蒸干得到Fe2O3固体:____________(第一步反应)
II.向2份0.1mol/LCH3COONa溶液中分别加入少量NH4NO3、Na2CO3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为_______、______(填“减小”、“增大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用序号填写下列空格:
①O2和O3②H2、D2和T2③12C和14C④石墨和足球烯(C60)⑤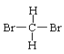 和
和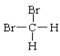 ⑥正丁烷和异丁烷⑦
⑥正丁烷和异丁烷⑦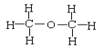 和
和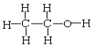 ⑧CH3CH3和CH3CH2CH2CH3
⑧CH3CH3和CH3CH2CH2CH3
互为同素异形体的是___;互为同位素的是__,互为同分异构体的是__,互为同系物的是__,同一种物质的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解法制备硼酸[H3BO3或B(OH) 3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的是( )

A. 阴极与阳极产生的气体体积比为1:2 B. b极的电极反应式为2H2O-2eˉ=O2↑+4H+
C. 产品室中发生的反应是B(OH)3+OHˉ=B(OH)4ˉ D. 每增加1 mol H3BO3产品,NaOH溶液增重22g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据反应:2Ag+(aq)+Cu(s)=Cu2+ (aq)+2Ag(s)设计的原电池如下图所示。

请回答下列问题:
(1)电极X的材料是___________,电解质溶液Y是___________;
(2)银电极为电池的___________极,发生的电极反应为___________;X电极上发生的电极反应为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com